В исследованиях физиологии микроорганизмов актуальным является изучение на клеточном и популяционном уровнях закономерностей регуляции энергозависимых процессов дыхания, питания, роста и размножения клеток [1]. Несомненное преимущество в этих исследованиях имеют быстро регистрирующие, высокочувствительные методы, позволяющие в адекватных условиях эксперимента получать кинетические характеристики ответных реакций изучаемого объекта на внешние воздействия. К числу таких методов относится полярографическое исследование дыхательной активности бактерий [2, 3].
Дыхание как терминальный этап катаболических реакций клетки, дающий интегративную характеристику всем звеньям окслительного метаболизма и поставляющий основную часть энергии у аэробных и факультативно-анаэробных бактерий, заслуживает самого пристального внимания при изучении их физиологического состояния. Однако у микробиологов сформировалось критическое отношение к такому параметру дыхания, как абсолютная (валовая) скорость потребления кислорода при окислении эндогенных или экзогенных субстратов [4, 5]. В то же время, в классической физиологии [6], и в частности, при исследовании функционального состояния митохондрий [7] применяются способы оценки энергетической эффективности окислительных процессов с использованием относительных параметров дыхания исследуемых объектов.
Попытки применения для изучения физиологии бактерий методических приемов, разработанных в митохондриологии, прежде всего, способа выявления дыхательного контроля (ДК) по Чансу-Уильямсу [8] моделированием ауторегулируемой последовательности метаболических состояний при добавлении в среду инкубации клеток экзогенного аденозиндифосфата (АДФ) не имели успеха [5, 9].
Вышеизложенное предопределило разработку альтернативных вариантов выявления дыхательного контроля у бактерий: по величине стимуляции дыхания клеток разобщителем карбонилцианид-р-трихлор- метоксифенилгидразоном [5], а также субстратами ∆µн+-зависимой транслоказы ß-галактозидов (лактозой, мелибиозой, тиометил-β-D- галактозидом) [9]. Сообщалось также о возможности выявления энергоразобщенных мутантов E.coli по их чувствительности к действию колицина К [10].
В процессе теоретической проработки обозначенной проблемы наше внимание привлекло то обстоятельство, что для бактериальной клетки каксложноорганизованной биологической системы характерна энергозависимая согласованность в регуляции ферментативных систем транспорта, гликолиза, цикла Кребса и дыхательной цепи [11, 4, 12]. Один из примеров общей координации различных звеньев метаболизма в соответствии с энергетическими запросами бактериальной клетки - это эффект Пастера, в основе которого лежит конкуренция двух метаболических систем (дыхание и гликолиз) за акцептор фосфата АДФ [1, 12].
Известен также обратный пастеровскому - эффект угнетения дыхания клеток гликолизом, обнаруженный при инкубации срезов некоторых перевиваемых опухолей в аэробных условиях в присутствии глюкозы [13, 14]. Первая фаза – стимуляция дыхания и окислительного фосфорилирования в результате быстрого использования АТФ в гексокиназной реакции и освобождения больших количеств АДФ - начинается через 1 с после добавления глюкозы в среду и длится около 2 мин. Вторая фаза – глубокое угнетение дыхания - длится 15…20 мин (Крэбтри-эффект). Опухолевые клетки, обладающие высокой гликолитической активностью, могут быть выведены из угнетенного состояния либо новым добавлением глюкозы, либо действием разобщающих агентов [15].
Наше внимание в данном явлении двухфазности дыхания клеток, окисляющих глюкозу, привлек механизм обратной связи концентрации АТФ и скорости потребления кислорода.
Цель работы - изучить динамику потребления кислорода бактерий при окислении ими глюкозы in vitro и на основании полученных закономерностей ауторегуляции дыхательной активности предложить способ выявления метаболического дыхательного контроля у пробиотических бактерий.
Задачи исследования:
- теоретически обосновать перспективность исследований функционального состояния бактерий методом оценки энергетической эффективности окислительных процессов с использованием относительным параметрам дыхания исследуемых объектов;
- экспериментально показать возможность применения разработанного способа для оценки функционального состояния бактерий развивающихся микробных культур.
Методика исследования: экспериментально-аналитическая. С использованием изготовленной в лабораторных условиях установки для полярографической регистрации скорости убыли кислорода из среды инкубации с бактериями, применяя поляризующийся платиновый электрод открытого типа [3]. В качестве среды инкубации использовали фосфатный буфер Na2HPO4ZNaH2PO4 (рН 6,7), содержащий 1 мМ MgCl2∙6H2O. Рабочий объем полярографической ячейки – 2 см3.
Материалы и методы
В работе использовали пробиотические микробные культуры, выращенные на плотных и жидких питательных средах на основе гидролизатов мяса и казеина.
Штаммы микроорганизмов. В работе использовали пробиотические микроорганизмы Escherichia coli М-17 и Lactobacillus plantarum 8РА-3.
Питательные среды. Для выращивания бактерий использовали жидкие и плотные питательные среды на основе гидролизатов мяса и казеина. В качестве среды инкубации при исследовании дыхания бактерий использовали приготовленный на дистиллированной воде фосфатный буфер Na2HPO√NaH2PO4 (рН 6,7), содержащий 1 мМ MgCl2∙6H2O.
Микробиологические, физико-химические и статистические методы. В качестве среды инкубации при исследовании дыхания бактерий использовали приготовленный на дистиллированной воде фосфатный буфер Na2HPO4∕NaH2PO4 (рН 6,7), содержащий 1 мМ MgCl2∙6H2O. Исходная концентрация кислорода в среде инкубации составляла 240 нмоль О2. Дыхательную активность измеряли при температуре (27±1)0С. Скорости дыхания (V) рассчитывали по количеству кислорода, потребленного 1 миллиардом жизнеспособных клеток за 1 минуту (нмоль О2/млрд. кл.·мин). Биологическую концентрацию (КОЕ) клеток определяли общепринятым "чашечным" методом, высевая разведенные клеточные культуры на плотную питательную среду в чашках Петри и подсчитывая число колоний через трое суток выращивания при температуре (27±1)0С. Растворы субстратов, разобщителей и ингибиторов дыхания готовили на среде, идентичной по составу среде инкубации. Гликолитическую активность бактерий определяли при температуре (27±1)0С по скорости закисления клеточных суспензий, приготовленных путем разведения исходных культур в объемном соотношении 1:5 физиологическим раствором NaCl. В качестве субстрата использовали глюкозу в конечной концентрации 1∙10-4 М. Скорость закисления регистрировали по показаниям рН-метра с записью на диаграммную ленту.
Содержание глюкозы в пробе при определении скорости потребления углевода бактериями измеряли с помощью анализатора глюкозы фирмы "Beckman", США.
В работе использовали изготовленную в лабораторных условиях установку для полярографической регистрации скорости убыли кислорода из среды инкубации с бактериями, применяя поляризующийся платиновый электрод открытого типа [3]. Рабочий объем полярографической ячейки – 2 см3.
Статистическую обработку результатов измерений проводили в соответствии с рекомендациями Г.Ф.Лакина [16], вычисляя средние арифметические значения показателей и доверительные интервалы их отклонений ( Х±195) для уровня вероятности 95%. Достоверность различийпри необходимости определяли, сравнивая расчетные (ţфакт.) и табличные (íстат.) значения критерия Стьюдента.
Результаты исследования и их обсуждение.
Наши попытки зарегистрировать на полярограмме дыхания ауторегулируемую последовательность метаболических состояний бактерий добавлением в среду инкубации АДФ не имели успеха, что согласуется с данными литературы [5] и подтверждает невозможность использования методических приемов, разработанных в митохондриологии, для выявления дыхательного контроля (ДК) по Чансу- Уильямсу у бактерий.
Изучая динамику потребления кислорода при окислении бактериями глюкозы, нам удалось, путем перехода на более низкие концентрации углевода, наблюдать смену фазы активного дыхания (V3), наступающей через 2…3 с после добавления субстрата, более медленной фазой окисления (V4). Разобщитель 2,4-динитрофенол (2,4-ДНФ) частично снимает эффект торможения, однако, не во всех опытах. Повторная добавка глюкозы приводит к новой стимуляции дыхания и последующему его торможению.
Проведя несложные расчеты, можно убедиться, что для полного окисления 25 нмоль глюкозы с образованием конечных продуктов СО2 и Н2О требуется 150 нмоль кислорода. Фактически за период фазы быстрого окисления глюкозы бактерии потребляют, как правило, 30…40 нмоль кислорода (‰). Однако в некоторых опытах мы не наблюдали торможения дыхания бактерий и после потребления 150 нмоль О2, либо это торможение было слабо выражено. В других опытах, напротив, торможение было значительным.
Наблюдаемые порой существенные отклонения от стехиометрически рассчитанных и экспериментально установленных усредненных данных, а также отсутствие, в ряде случаев, двухфазности процесса дыхания клеток, окисляющих глюкозу в низких концентрациях, явились предпосылкой для более детального изучения данного явления.
Интактные клетки бактерий всегда содержат определенное количество эндогенных субстратов, АТФ и АДФ, а Рнеорг., по условиям наших экспериментов, находится в избытке в среде инкубации. Первичные этапы катаболизма глюкозы у бактерий включают транспорт углевода и превращение его в глюкозо-6-фосфат и фруктозо-1,6-дифосфат. Поскольку эти процессы требуют затраты энергии АТФ, можно предположить, что внутриклеточное отношение [АТФ]/[АДФ] у бактерий уменьшается, а активация дыхания в значительной мере обусловлена окислением эндогенных субстратов в дыхательной цепи (ДЦ) для компенсации низкоэнергетического сдвига. Для подтверждения этого предположения в предварительных опытах с 8 микробными культурами мы убедились, что продолжительность фазы активного дыхания (τ) бактерий, окисляющих 25 нмоль глюкозы, совпадает по времени с продолжительностью ее полного потребления клетками из среды инкубации (2,39±0,19 и 2,27±0,17 мин соответственно).
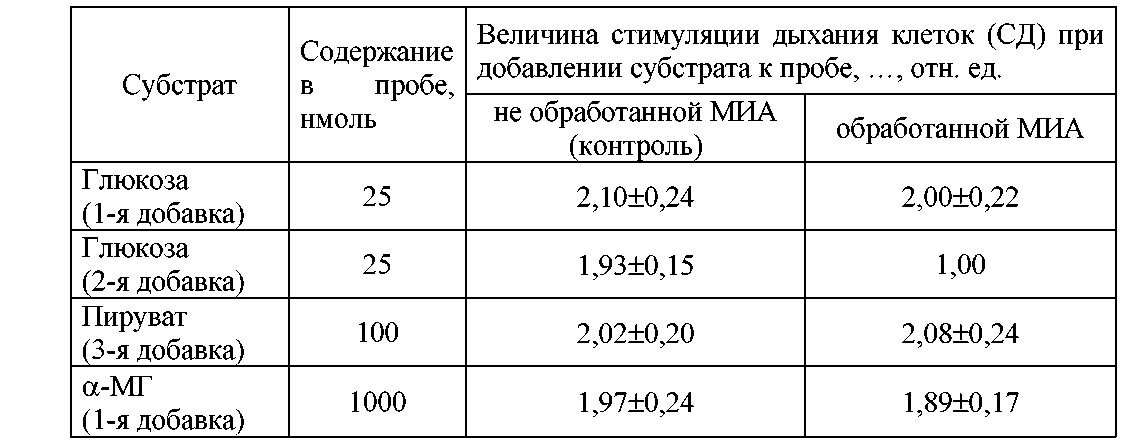
Другими свидетельствами справедливости высказанного предположения явились результаты оценки влияния ингибирования гликолиза моноиодацетатом натрия (МИА) на эффект стимуляции дыхания клеток пируватом, глюкозой и ее биохимическим аналогом ɑ-метил-ß-D- глюкопиранозидом (ɑ-МГ), метаболизм которого ограничивается первичными актами фосфорилирования при его переносе в клетки бактерий (таблица 1), а также данные опытов с энергизующими и деэнергизующими воздействиями на клетки Y.pestis (таблица 1).
Таблица 1 – Влияние ингибирования гликолиза моноиодацетатом натрия (МИА) на стимуляцию дыхания Escherichia coli М-17 различными субстратами ( X±I95, n=7)
Совпадение продолжительности активного дыхания и продолжительности аккумуляции 25 нмоль глюкозы, а также результаты, представленные в таблице 1, позволяют полагать, что активация дыхания бактерий при добавлении микроколичеств глюкозы связана не столько с окислением экзогенного углевода, сколько с инициацией окисления эндогенных субстратов, компенсирующего затраты энергии на транспорт и первичные реакции фосфорилирования утилизируемого углевода. Фаза активного дыхания (состояние 3) продолжается, по крайней мере, до тех пор, пока происходит энергопотребляющий процесс утилизации глюкозы, т.е. создаются условия для сдвига равновесия реакции "фосфорилирование АДФ о дефосфорилирование АТФ" в правую сторону.
Ауторегулируемый переход бактерий, окисляющих глюкозу, в состояние "отдыха" (состояние 4) после периода активного дыхания представляет собой наиболее интересный и информативный аспект изучения энергетической регуляции окислительного обмена.
Используя, в основном, способы расчета параметров, принятые в митохондриологии, а также устоявшуюся терминологию, степень
ауторегулируемого торможения дыхания исследуемых бактерий мы также охарактеризовали показателем МДК (метаболический дыхательный контроль). Для подтверждения его информативности в качестве добавок, снижающих энергизованность клеток, использовали разобщитель – протонофор 2,4-ДНФ (1 · 10-4 М) и неметаболизируемый аналог глюкозы ɑ- МГ (1·10-2 М),энергозависимый транспорт которого в клетки связан с затратами энергии АТФ [5, 9]. Избирательное ингибирование протонтранслоцирующей аденозинтрифосфатазы (АТФ-азы) дициклогексилкарбодиимидом (ДЦКД) в концентрации 5·10-3 М, напротив, способствует энергизации клеток в экспоненциальной фазе развития, когда активность данного фермента наиболее высока [15]. Результаты исследования закономерностей ауторегуляции дыхательной активности Y.pestis под влиянием энергизующих и деэнергизующих добавок представлены в таблице 2.
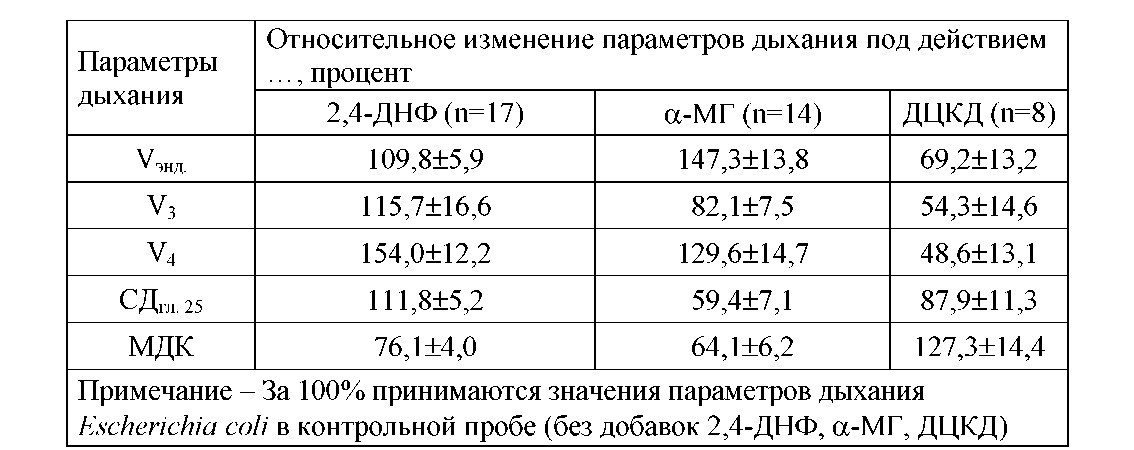
Таблица 2 – Изменение параметров дыхания Escherichia coli М-17 под действием разобщителя 2,4-динитрофенола (2,4-ДНФ), неметаболизируемого ɑ-метил-ß-⑉-глюкопиранозида (ɑ-МГ) и ингибитора АТФ-азы дициклогексилкарбодиинида (ДЦКД), ( X±I95)
Из данных таблицы 2 следует, что воздействия, приводящие к разобщению окислительного фосфорилирования и деэнергизации клеток, вызывают ослабление ауторегулируемого торможения окислительной активности бактерий, что проявляется в увеличении скорости дыхания микроба в метаболическом состоянии 4 (V4) и в снижении величины МДК. Напротив, энергизация клеток, обработанных ДЦКД, приводит к достоверному снижению скорости дыхания в состоянии "отдыха" (V4) и достоверному увеличению значения МДК. Разнонаправленный характер изменения других параметров дыхания в этих опытах взаимно не согласован и не поддается однозначной трактовке.
Следующим шагом в проверке информативности и значимости параметров дыхания, рассчитываемых на основании исследования
ауторегулируемой последовательности метаболических состояний бактерий, явилось изучение дыхательной активности развивающейся популяции, традиционно используемой физиологами как модель, с помощью которой отрабатываются критерии физиологического состояния микробных культур [8, 17]. Активное размножение бактерий в
экспоненциальной фазе роста периодической культуры требует значительных энерготрат, что, в свою очередь, обусловливает высокую скорость биоэнергетических процессов. Переход в стационарную фазу, напротив, сопровождается снижением скорости накопления биомассы и, следовательно, значительным уменьшением энерготрат на биосинтезы; энергизованность покоящихся клеток при этом возрастает.
Обобщенные результаты опытов с десятью культурами Escherichia coli М-17, выращиваемыми в 10¯литровом аппарате с аэрацией при температуре (27±1)0С и рН 6,7±1,0, показали, что в лаг¯периоде развития культур (до 6 ч от начала выращивания) происходит некоторое снижение концентрации живых микробов. В этот же период значительно увеличиваются удельная скорость эндогенного дыхания, снижаются величины параметров СДгл. 25 и МДК. Показатель МДК к концу лаг¯ периода и началу экспоненциальной фазы роста (6…9 ч от начала выращивания) принимает, как правило, значения, близкие к минимальному (1,00).
Во время экспоненциальной фазы роста, по мере накопления биомассы, происходят снижение удельной скорости эндогенного дыхания, более выраженное к 12…15 ч культивирования, а также увеличение значений параметров СДгл. 25 и МДК вплоть до окончания культивирования. Через 9…12 ч от начала выращивания бактерии проявляют сначала слабую, а с увеличением продолжительности культивирования – более выраженную способность стимулировать дыхание под действием разобщителя 2,4¯ДНФ, что свидетельствует об увеличении трансмембранного градиента протонов.
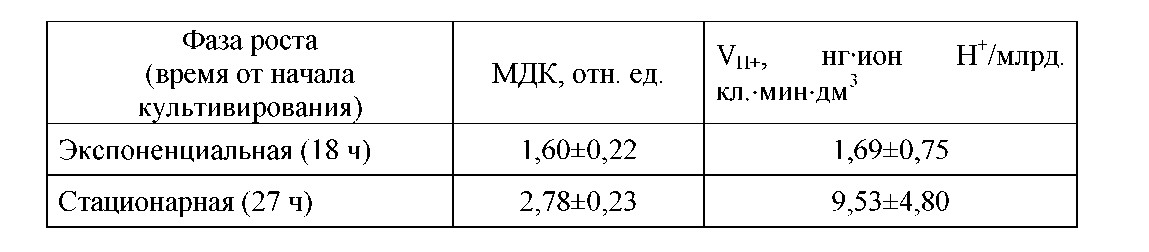
В стационарной фазе роста культуры характеризуются наиболее низкими за весь цикл развития скоростями окисления эндогенных субстратов. К концу стационарной фазы роста (27 ч культивирования) ауторегуляция дыхательной активности клеток по показателю МДК достигает максимальных значений и достоверно (ţфакт=8,38; ţстат=2,10) отличается от ее значений в экспоненциальной фазе роста. Характерно, что к 27 ч культивирования достоверно (ţфакт.=3,65; ţстат=2,10) возрастает и удельная гликолитическая активность клеток, о чем свидетельствуют данные таблицы 3.
Таблица 3 ¯ Степень ауторегуляции дыхания (МДК) и удельная гликолитическая активность (Vh+) культур Escherichia coli М-17 в различных фазах периодического выращивания ( X±I95, n=10)
Изменения физиологического состояния клеток в экспоненциальной и стационарной фазах развития периодической культуры, характеризуемые по другим параметрам дыхания, оцениваются как статистически малодостоверные. Характерно, что прекращение аэрации и перемешивания культур, а также снижение температуры до (20±2)0С в последующие 3 ч (27…30 ч) приводят к существенному (почти в 2 раза) возрастанию МДК, причем, как следует из данных, приведенных на рисунке 2, уровень стимуляции дыхания глюкозой значительно уступает уровню его последующего угнетения (СД гл.25 < МДК). Последнее свидетельствует о том, что переживание культур, достигших физиологической зрелости, приводит к резкому снижению энерготрат на их поддержание и, как следствие, к увеличению энергизованности бактерий.
Физиолого-биохимический смысл регистрируемых эффектов заключается в том, что в условиях снижения энерготрат (по завершении стационарной фазы развития) переживающая популяция бактерий переключает свой метаболизм на менее энергопродуктивный - гликолитический путь, усиливая одновременно метаболический (аденилатный) контроль за дыхательной активностью клеток. Через 10…12 часов переживания культур без перемешивания в захоложенном до температуры 8…100С состоянии мы наблюдали последовательное увеличение МДК до максимального значения 9,50 и далее - эффект полного прекращения стимуляции дыхания клеток глюкозой (СД гл.25 = 1,00), которая обратимо восстанавливалась интенсивной аэрацией культур.
Выводы:
Результаты свидетельствуют о том, что исследование ауторегулируемой последовательности метаболических состояний бактерий и расчет величины метаболического дыхательного контроля (МДК) являются информативным способом изучения закономерностей регуляции дыхательной активности и физиологического состояния.
Литература
- Асонов Н.Р. Микробиология. 4-е изд., перераб. и доп. Колос, М. 2001.
- Лукьянова Л.Д., Балмуханов Б.С., Уголев А.Т. Кислородзависимые процессы в клетке и ее функциональное состояние. Наука, М.1982.
- Руководство по изучению биологического окисления полярографическим методом. Под ред. Г.М.Франка. Наука, М. 1973.
- Минкевич И.Г., Ерошин В.К. Закономерности внутриклеточного материально-энергетического баланса роста микроорганизмов. Успехи соврем. биол. 82(1): 103-116. 1976.
- Burstein C., Tiankova L., Kepes A. Respiratory control in Escherichia coli K 12. Eur. Ĵ.Вİосĥет. 94: 387-392. 1979.
- Ноздрачев А.Д., Баженов Ю.И., Баранникова И.А., Батуев А.С. и др. Начала физиологии: Учебник для вузов. Под ред. акад. А.Д.Ноздрачева. Изд-во "Лань", СПб. 2001.
- Патологическая физиология. Учебник для мед.вузов. Под ред. А.Д.Адо, М.А.Адо, В.И.Пыцкого, Г.В.Порядина, Ю.А.Владимирова. Триада-Х, М. 2000.
- Chance B., Williams G.R. The respiratory chain and oxidative phosphorylation. Adv. Enzymol. 17: 65-134. 1956.
- Tsuchiya T., Rosen B.P. Respiratory control in Escherichia coli. FEBS Lett. 120(1): 128-130. 1980.
- Plate C.A. Colicin K as a probe of energy coupling in Escherichia coli. Microbiology. 1979. Ed. D.Schlessinger. Washington. D.C. 58-61. 1979.
- Лукоянова М.А., Тихонова Г.В. Организация дыхательной цепи и аккумуляция энергии у бактерий. Итоги науки и техники. Сер. Биол. химия. ВИНИТИ, М. 17:33-74. 1982.
- Стейниэр Р., Эдельберг Э., Ингрэм Д. Мир микробов. Т.1. Пер. с англ. Под ред. Е.Н.Кондратьевой. Мир, М. 1979.
- Рэкер Э. Биоэнергетические механизмы: новые взгляды. Пер. с англ. Под ред. В.П.Скулачева. Мир, М. 1979.
- Сейц И.Ф. Взаимодействие дыхания и гликолиза в клетке и сопряженное фосфорилирование. Медгиз, Л. 1961.
- Хесс Б. Реакция компонентов дыхательной цепи в неповрежденных клетках. В кн.: Внутриклеточное дыхание. Фосфорилирующие и нефосфорилирующие реакции окисления. Труды 5 Международного конгресса. Изд-во АН СССР, М. 330-340. 1962.
- Лакин Г.Ф. Биометрия. Высшая школа, М. 1980.
- Neidhardt F. Bacterial growth: constant observation with dN/dt. J.Bacteriol. 181(24): 7405-7408. 1999.