Берілген мақалада ерігіштік сынамасының құрамында лоратадині бар генерик таблеткаларын салыстыру мысалдары көрсетілген. Ерігіштік қисық сызықтарынын байқайтынымыз лоратадиннің жақсы еритін ортасы, яғни pH 1,0 тұз қышқылы еріткішті қолдану арқылы жасалған зерттеулерде қисық сызықтардың бір-бірінен айырмашылықтары бар екенін көре аламыз. Лоратадин белсенді затының төменгі pH көрсеткіштерінде дәрілік қалыптан жақсы босап шығатынын дәлелдейді.
Кіріспе. Аллергиялық сырқаттардың созылмалы және өткір кезеңдерінде лоратадин препараттары өте кең ауқымда қолданылады. Ауыз қуысы арқылы қолданылатын лоратадин дәрілік қалыптары, әсіресе таблеткаларының биожеткіліктілігі өте жоғары болып келеді [1].
Бірақ көп байқалатын құбылыс болып терапевтикалық әсеретуінде айырмашылықтар байқалады, бұл жағдайды генерик таблеткалардағы лоратадиннің дәрілік қалыптан босап шығу жылдамдығымен түсіндіруге болады [2].
Қайта жасалған дәрілік қалыптардың биоэквиваленттілігін растайтын бірден-бір сынама осы ерігіштік сынамасы болып келеді және бұл айырмашылық және ұқсастық мәселесінің шешуші факторы болып табылады [3].
Мақсаты. Мақаланың мақсаты болып «ерігіштік» сынамасын жүргізу арқылы лоратадин генерик препараттарын бір-бірімен салыстыра отырып, дайындалған минитаблеткалардың биожеткіліктілігін анықтау болып табылады [4].
Соңғы кездерде аталмыш сынаманы in vivo зерттеулерінде қайта жасалған дәрілерге салыстырмалы сынама ретінде қолдану да ұсынылатын болды. Белсенді заттың дәрілік қалыптан босап шығуына екі түрлі фактордың әсер ететінін білеміз [5]: субстанцияның физика- химиялық қасиеттері (ерігіштігі, бөлшек өлшемдері, кристалдық күйі) және дәрілік қалыпқа тәуелді факторлары (дайындау технологиясы, қосымша заттары). FDA ақпараты бойынша [6] өндіріс үшін қатты дәрілік қалыптарға ерігіштік сынамасын жасауға 1995 жылы ұсынылған ішіне дәрілік заттың ерігіштігі мен оның асқазан ішек жолдарында сіңуі кірген дәрілік заттың биофармацевтикалық жіктелуі кіреді. Барлығымызға белгілі болғандай «жақсы ериді» деп pH 1–8 мәнінде 250 мл буферде белменді заттың барлық мөлшері еріп кеткенді айтады. Сонымен қатар «жақсы сіңеді» деп асқазан-ішек жолдарынан белсенді заттың 90 % - дан кем емес мөлшерінің сіңуін айтады[7].
Осыған байланысты келесі жіктеулерді білеміз:
- жақсы ериді + жақсы сіңеді;
- жаман ериді + жақсы сіңеді;
- жақсы ериді + жаман сіңеді;
- жаман ериді + жаман сіңеді.
Ерігіштік сынамасы бойынша зерттеудің ең қарапайым түрі болып екінші топтагы дәрілік заттар табылады, өйткені дәл осыларға субстанцияның бөлшек мөлшері, кристалдық күйі, дәрілік қалыптың түри мен қасиеті әсер етеді. Зерттеу барысында қарқынды қызығушылықты шақыратын бірінші және үшінші топ заттары болып табылады[8]. Дәрілік қалып қасиеті, субстанцияның бөлшек мөлшері және кристалдық күйі бұл жағдайда дәрілік заттың босап шығуына өте үлкен әсер ете қоймайды, сондықтан бұл дәрілік заттыр үшін ерігіштік сынамасының құны қанша деген сұрақ туындайды. Сондықтан осы мәселені шешу мақсатында зерттеу нысанасы ретінде H1 –гистамин рецепторларының блокаторы дәрілік зат тобы, оның ішінде лоратадин таңдалып отыр. Лоратадин молекуласының құрамында негізгі орталық – ароматты пиридин азот атомының ( сурет 1) болуы – бұл заттың қышқылды минерал еріткіштерде жақсы еритінін білдіреді.
Лоратадин суда мүлде ерімейді деуге болады. Асқазан сөлі ортасында, яғни pH 1-4 аралығында негізгі азот атомы иондалған қалпында болғандықтан лоратадин осы ортада жақсы ериді.
Ауыз қуысы арқылы қабылданған лоратадиннің биожеткіліктілігі айтарлықтай жоғары [9]. Сондықтан да бұл дәрілік затты биофармацевтикалық жіктеудің бірінші тобына жатқызуға болады.
Тәжірибелік бөлім. Зерттеу нысаналары ретінде құрамында белсенді зат лоратадині бар әртүрлі өндірушілердің таблеткалары қолданылды: Кларисан 10 мг (Санто, Қазақстан), Лоратал, 10 мг («Нобель», Қазақстан), дайындалған минитаблеткалар, 1.0 мг. Ерігіштік тестісі фармакопеядағы «Ерігіштік» бабына сәйкес «лопасты араластырғыш» аппаратынмен «Pharmа test» қондырғысында жүргізілді. Еріту ортасының көлемі – 900 мл, температурасы – 37°С құрады. Лопасты араластырғыштардың айлану жылдамдығы – 80 айн/мин құрады. Еріткіш ортасы ретінде pH 1,0 тұз қышқылы ерітіндісі қолданылды. Орта рН – ының дайындалуын рН-метрдің көмегімен қадағалап отырдық. Зерттеулер әрбір препараттың алты түрлі үлгілеріне минитаблеткаларына жүргізілді. Сынамаларды алу уақыты тәжірибе басталған соң әрбір 1, 3, 5, 15, 30 мин сайын алып отырдық. Алынған сынама көлемі – 5 мл құрады. Сынама алынып болған соң сынамаға кеткен көлемді тура сондай көлемдегі тұз қышқылы ерітіндісімен толықтырып отырдық. Алынған сынамаларды еріткіш ортасымен сұйылтып, «ақ жіп» типті қағаз сүзгіш арқылы сүзгіден өткізіп, сүзілген фильтраттың бірінші бөлшегін төгіп тастап отырдық. Сандық анықтауды УК-спектрофотометрия әдісімен DT 800 типті спектрофотометр (Erweka , Франкфурт, Германия) құрылғысында 280 нм толқын ұзындығында жүргіздік. Салыстырмалы ерітінді ретінде сәйкес еріткішті қолдандық. Жүргізілген әрбір зерттеу үшін концентрациясы 10 мкг/мл-ге тең бөлек – бөлек стандартты үлгі ерітіндісін дайындадық. Стандартты ерітінділерді «ақ жіп» типті қағаз сүзгіш арқылы сүзгіден өткіздік (сынама ерітінділері тәрізді). Стандартты шарт жағдайда (лопасты араластырғыш айналу жылдамдығы 80 айн/мин, еріткіш ортасы – HCl pH 1,0 мәнімен, еріткіш ортасының көлемі – 900 мл, орта температурасы – 37°С) «Кларисан», «Лоратал» 10 мг және «минитаблеткалар» 1 мг таблеткаларынан лоратадиннің босап шығу қисық сызықтары алынды. Алынған зерттеу нәтижелеріне сәйкес (сурет 1) лоратадин құрамды таблеткалар ерітіндіге дегенмен тез өтетінін байқай аламыз 15 минуттың ішінде белсенді заттың 70% - дан кем емес мөлшері босап шығады, осыдан кейін ерігіштік жылдамдығы күрт төмендейді. Көбінесе пайда болатын жайт, босап шығу қисықтарының арасында ең айырмашылығы қатты байқалатын кездері болып ерігіштік тестінің 1 минуттық нүктесіндегі нәтижесі табылады. FDA ақпараттарына сүйенетін болсақ, бірінші және үшінші топтағы дәрілік заттың босап шығуын ерігіштік тестімен тексергенде алғашқы алынатын сынама нүктесі және аралары әрбір бес немесе он минутты құрау керек. Бұл дегеніміз модифицирленген емес дәрілік препараттарды тексеру барысында босап шығу алпыс – жетпіс минут ішінде ерігіштік қисығында кем дегенде алты нүктенің болуы тиіс. Қисықтар арасындағы айырмашылықты көзбен көру арқылы ажырата аламыз.
Алынған нәтижелерге сүйене отырып, дайындарған минитаблеткалардың босап шығуы нарықта бұрыннан келе жатқан препараттардан еш айырмашылығы жоқ дей аламыз.
Сонымен қатар босап шығу қисықтарын төменде көре аламыз.
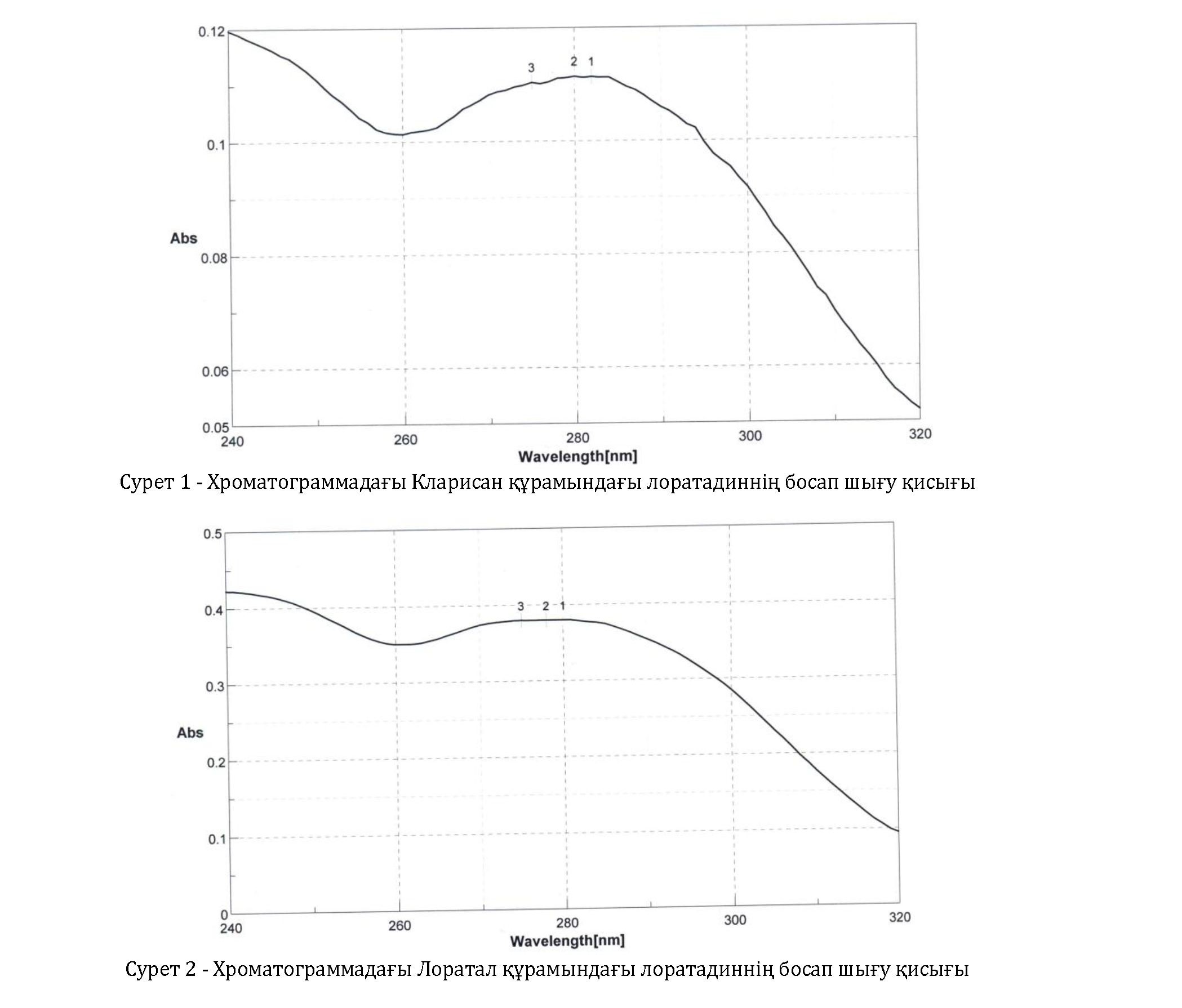
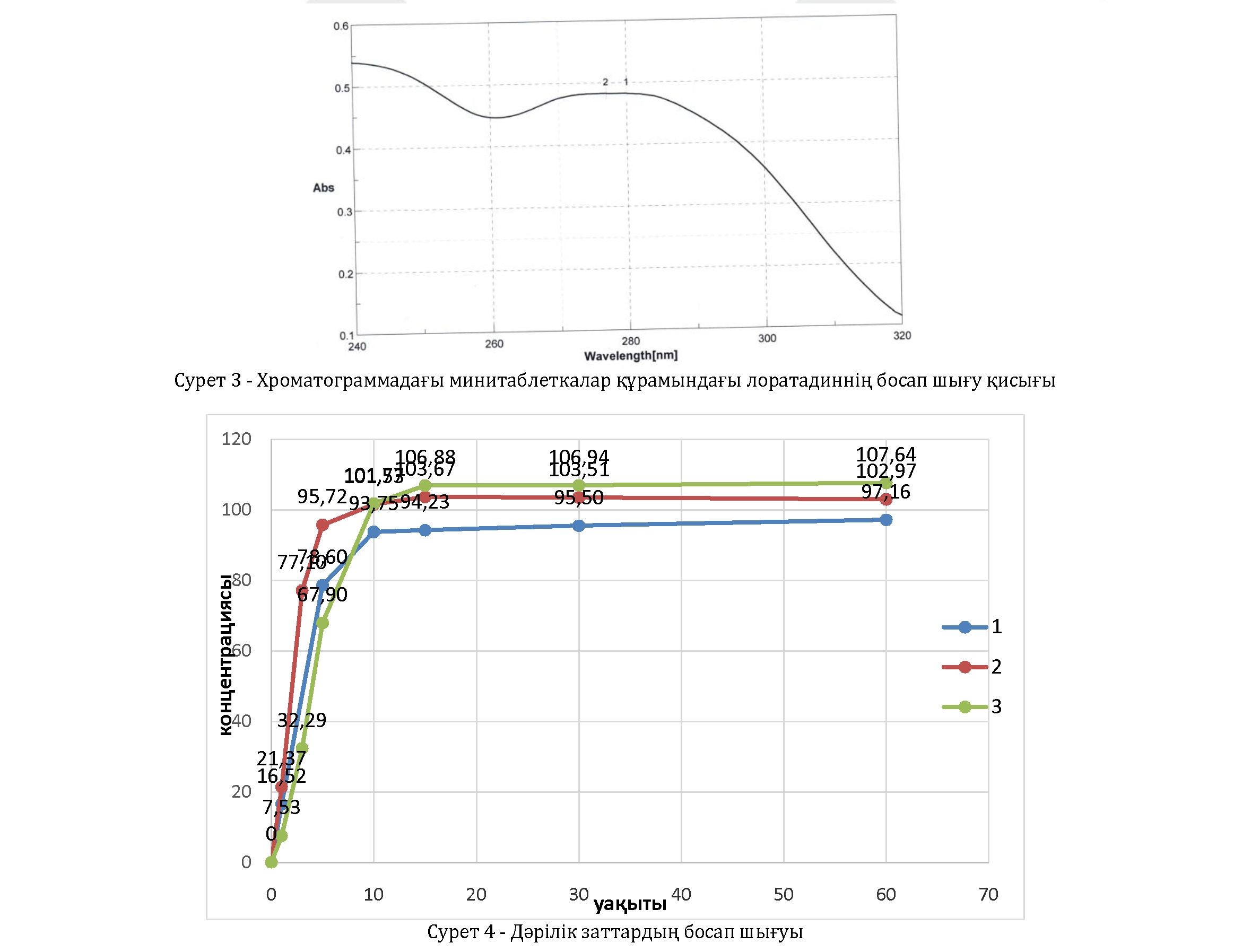
Жоғарыдығы диаграммада берілген 1 санымен белгіленген Кларисан 10 мг (Санто, Қазақстан) таблеткалары, 2 санымен белгіленген Лоратал, 10 мг («Нобель», Қазақстан) таблеткалары, ал 3 санымен белгіленген дайындалған минитаблеткалар, 1.0 мг. Соныммен диаграммада көрсетілгендей дайындалған таблеткалардың нарықта жақсы орныққан препараттардан еш айырмашылығы жоқ, демек, биожеткілігі талаптарға сәйкес деп нақ айтуға болады.
Қорытынды
Құрамында лоратадины бар генерик препараттарын салыстыру мақсатында айырмашылық және ұқсастық үрдістерін пайдалана отырып «ерігіштік» тестін қолдануға болатындығына көз жеткізе аламыз.
Құрамында лоратадины бар генерик препараттарын салыстыру барысында босап шығу қисықтарының бір-бірінен айырмашылығын еріткіш орта ретінде pH мәні 1,0 болатын тұз қышқылын қолдана отырып жүзеге асатынын біле аламыз.
ӘДЕБИЕТТЕР ТІЗІМІ
- А.П. Мешковский. Место дженериков в лекарственном обеспечении // Фарматека. - 2003. - № 3. - С. 103-108.
- M.E. Ruiz1, A. Gregorini1, A. Talevi et al. Dissolution Studies of Generic Medications: New Evidence of Deviations from the Transitivity Principle // Dissolution Technologies. - 2012. - Р. 13-24.
- Бекетов, Б.Н. Метрологические аспекты и биофармацевтческие исследования по анализу, технологии и эффективному применению лекарственных средств: автореф. дис. ... д-р. Фарм. Наук - Пермь, 2001. - 47 с.
- ГОСТ 52249-2004 "Правила производства и контроля качества лекарственных средств" от 2005.01.01. - М.: Изд-во стандартов, 2004. - 125 с.
- H. Kortejаrvi, R. Shawahna, A. Koski et al. Very rapid dissolution is not needed to guarantee bioequivalence for biopharmaceutics classification system (BCS) drugs // J Pharm Sci. - 2010. - V. 99(2). - Р. 621-625
- P. Langguth. Evaluation of bioequivalence of drug products // Pharm Ind. - 2009. - V. 71. - № 2. - P. 258-263.
- G.P. Martin, V.A. Gray. Overview of Dissolution Instrument Qualification, Including Common Pitfalls // Dissolution Technologies. - 2011. - P. 6-10.
- Q. Wang, D. Ma, J.P. Higgins. Analytical Method Selection for Drug Product Dissolution Testing // Dissolution Technologies. - 2006. - P. 6-13.
- S.А. Qureshi. Reporting and Analyzing Drug Dissolution Results: A Systematic Approach // Аm Pharm Rev. - 2010. - Р. 8185.