Ацетилен туындылары органикалық химия саласында маңызды ауылшаруашылық өнімдер мен биологиялық белсенді қосылыстарды алуда синтез бастамасы ретінде ерекше орынға ие. Олардың химиялық түрленуінің ерекшелігі энергиясы жоғары үштік байланысқа және қозғалмалы этинилдік сутегіге байланысты. Бұл жай ацетилендік қосылыстардың көптеген реакцияларға оңай түсу қабілетіне түсіндірме болып табылады және олардың әр түрлі биологиялық белсенділік көрсетуіне себеп болады. Сондықтан осы мақалада ацетилен туындыларының синтез ерекшеліктері мен маңызды биологиялық белсендігіне шолу жасалған.
Тақырыптың өзектілігі.Ацетилендік қосылыстардың жоғары әрі көпқырлы реакциялық мүмкіншілігі оларды әр түрлі тәжірибелік қолданысқа арналған молекулалық құрылымдар мен ансамбльдерді жобалау үшін оңтайлы блоктар етеді. Олардың биологиялық белсендігі негізінен үштік байланыстың реакциялық қабілеті мен зерттеліп жатқан молекуланың құрылысына тәуелді. Сондықтан осы таңда синтетикалық биологиялық белсенді қосылыстар арасында ацетилен туындыларының алатын үлесі зор. Соған орай құрамында үштік байланысы бар қосылыстардың синтез ерекшеліктері мен көрсеткен биологиялық белсендіктеріне анализ жасау маңызды.
Негізгі бөлім. Ацетилен туындыларынан жаңа молекулярлық құрылым алу үрдісі үштік байланыстың ашылуы немесе сақталуы арқылы жүзеге асады.Үштік байланыстың каталитикалық түрленуі негізінде стратегиялық маңызды, көптонналы органикалық синтез өнімдері - винилацетилен, ацетальдегид, акрилонитрил, хлорвинил, хлоропрен, пропаргил спирті және т.б. өнеркәсібі жолға қойылған. Күрделі ацетилендік құрылымдардың тәжірибелік тұрғыдан пайдалы қасиеттерге ие болуы молекуладағы функционалдық топтар мен үштік байланыстың табиғатына байланысты екені жалпы мәлім, сондықтан қазіргі таңда құрамына қос немесе үштік байланыстар кіретін үлкен биологиялық белсенді қосылыстар класы пайда болуы заңды. Олардың көпшілігі әртүрлі маңызды биологиялық қасиет көрсетіп, антибиотиктар, фунгицидтар және инсектицидтар ретінде қолданыс табуда [1].
Медицинадан бөлекацетилен туындыларының кейбіреулері молекулярлық электрониканың элементтері ретінде, анықтау молекулалары, Ленгмюр-Блоджетт пленкалары ретінде де қолданылады [2].
[3] шолуында жаңа дәрілік заттарды әзірлеудегі әртүрлі стратегияларды бағалау үшін келесі мәліметтер келтірілген: «өткен онжылдықтарда жыл сайын шамамен 50-60 жуық жаңа препараттар тіркеліп, клиникалық практикаға енгізілген болса, соңғы жылдары енгізілген жаңа препараттар саны күрт азайып, 2000 жылы - 27, 2001 - 24 және 2002 - 18 қосылыспен өзінің минимумына жеткен».Бұл Қазақстан үшін ерекше маңызды, себебі елімізде өндірілген медицинада қолданылатын дәрілік препараттардың мөлшері 5¿ аз, ал отандық ауыл шаруашылығында қолдануға рұқсат етілген өсімдік қорғау химиялық қосылыстар саны екеу-ақ.
Осы жұмыста Глязер мен Ходкевич-Кадио бойынша ацетилен туындыларының қышқылдық конденсациясы қарастырылмаған, себебі ол жайлы ақпараттар монографияда толық келтірілген [4].

жалғастырылды [7]. Сол жұмыстар Қазақстанда ацетилен және қаныққан кетондар химиясының іргетасы қаланып, жаңа полициклды қосылыстарды алу үшін аминдер, амидтер және бромидтерді ауыл өсуін тапқан, өсімдік стереобағытталуын зерттеу, соған қоса ароматты окси(амино)-пропаргилдердің, моно- және бициклді кетондармен байланысы жұмыста автормен толығырақ келтірілген [5].
Қазақстанда пропаргилді қосылыстар химиясы саласында алғашқы жұмыстар ҚазССР ҒА, х.ғ.д. профессор И.Н. Азербаев басшылығымен басталған болатын. Оның ғылыми зерттеулерінің ретроспективті анализі мен осы бағытта алған зерттеу нәтижелері [6] шолуда көрсетілген. Кейіннен осы зерттеулер А.Б. Бектұров атындағы химия институтының физиологиялық белсенді қосылыстар химиясы лабораториясында х.ғ.д., профессор Қ.Б. Ержанов басшылығымен нәтижесінде гетероциклді
Бұл жұмыста пропаргил пентосилоундекан және амантадинмен әрекеттестірген. Синтездеген заттардың нейропротекторлық қасиеттерін анықтау барысында 88-фенил-этинил-8- гидроксипентациклоундекан,фенилпропаргил орынбасары шаруашылығында қолданыс реттегіштер мен биологиялық белсенді қосылыстар алынды [8].
Жоғарыда айтылған себептерге сүйенсек, аталмыш бөлімде соңғы жылдардағы ароматты пропаргилді эфирлердің синтезі жайлы әдеби мағлұматтар жинақталған.
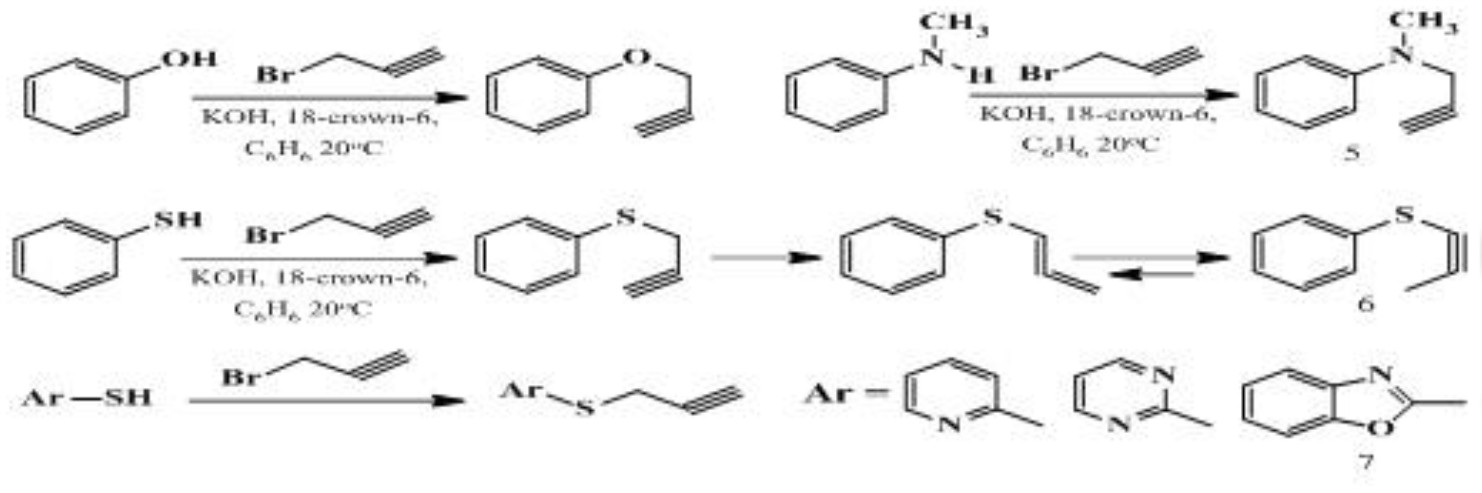
Рубина К. мен Флейшер М. бастаған ғалымдар фенол, тиофенол, N-метиланилин, 2-пиридинтиол, 2-
пиримидинтиол мен 1,3-бензоксазол-2-тиол 5 - 7пропаргил туындыларының синтезін жүзеге асырған. Фаза аралық катализ жағдайында (2-пропинил)-фенилсульфид 6 алленилфенилсульфид пен (1-пропинил)фенилсульфидке изомерленеді. Қайта топтасу реакциясының механизмі квантты-химиялық «АМ1» әдісі арқылы зерттелген [9].
бар қосылыс ең жоғары белсенділік көрсетті. Ол МАО-В (моноамин оксидаза-В) энзимын 300 мкг/мл концентрацияда 73,32 ¿ ингибирледі, яғни бұл қосылыс паркенсон ауруын емдеуге потенциалды қосылыс болып табылады [10].
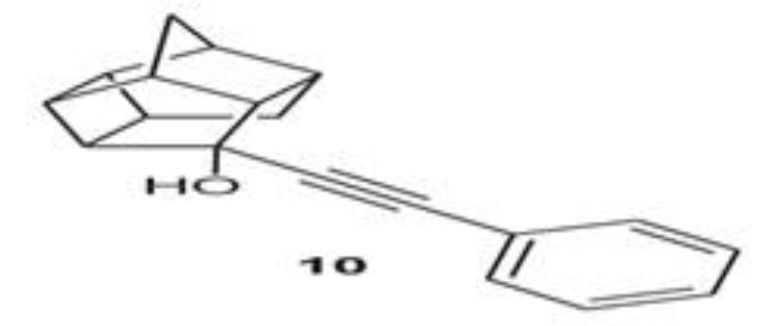
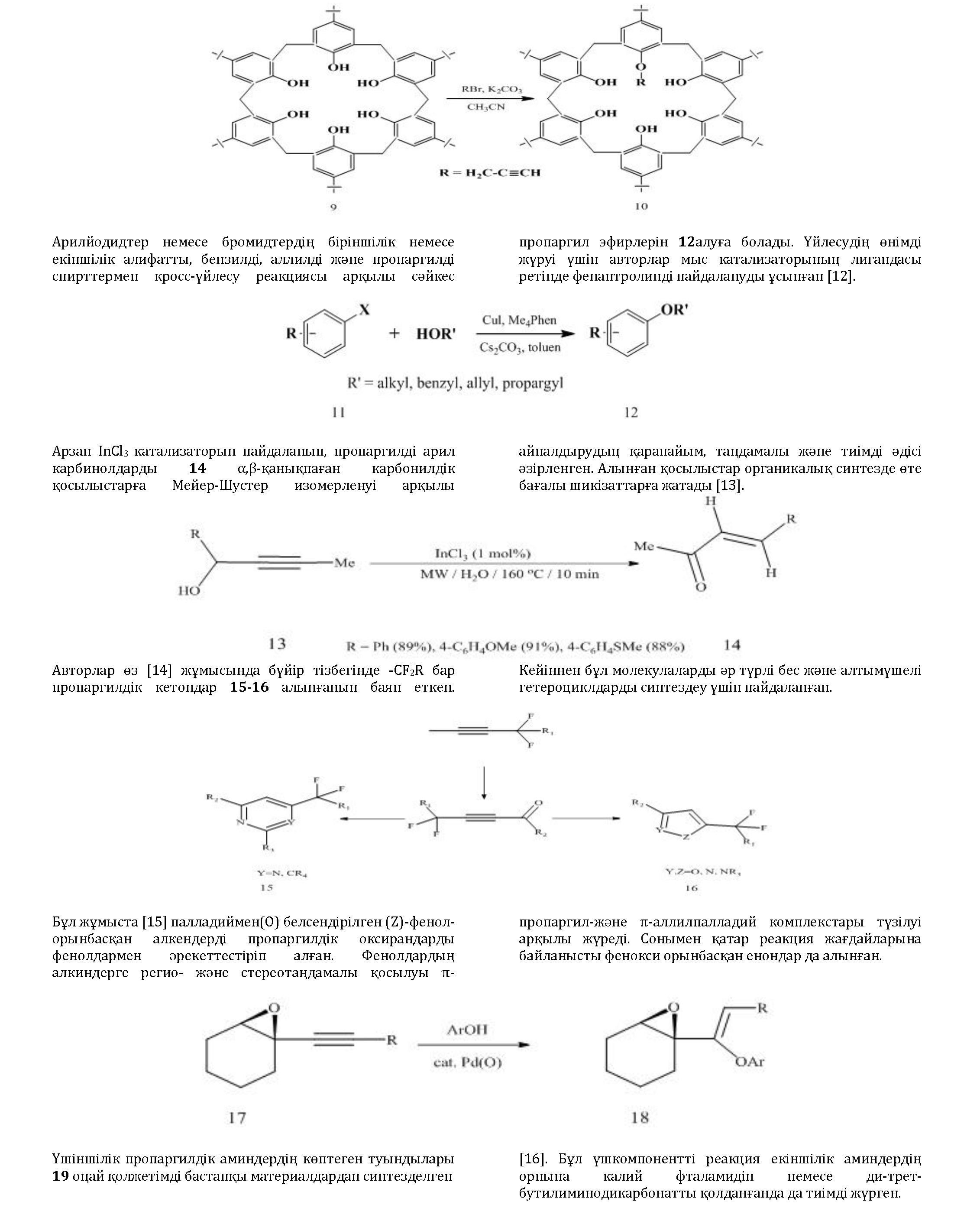
Бұл жұмыста [11] жақсы шығыммен моноалкилді эфир 4- трет-бутилкаликс[6]ареннің региоселективті синтезі жүзеге асырылған. Бұл реакцияның әдеттегі жағдайларда шығымы 53¿ болатын. 20 °С температурада ультрадыбыспен әсер ету жағдайында, негіз ретінде 2,2 эквивалентті натрий карбонатын пайдалана отырып, ацетонитрилге бромды пропаргилді қосқанда, 10эфирі түзілген.
көптеген табиғи антибактериялық, да биологиялық тараған құрылымдық блоктар болып табылады және маңызды биологиялық қасиеттер көрсетеді, әсіресе, саңырауқұлақтарға қарсы. Соңғы онжылдықтарда дииндар органикалық молекулалық материалдардағы маңызды функционалды блоктар ретінде мойындалып, нанометрлік масштабтарда молекулалық сымдар мен молекулалық архитектура бөлігі ретінде орнықты [29]. Қосарласқан дииндар мен полииндар қосылыстардың құрамына кіріп, саңырауқұлақтарға қарсы және басқа 8-Метокси-3-фенил-5-метилпропаргиламинометил-2Н-1- бензопиран-2-он [27] қосылысы улылығы төмен антибактериялық қасиет көрсететін фармацевтикалық препарат ретінде ұсынылған.
Алкиндер көптеген синтетикалық өнімдер мен жаңа материалдардағы құрылыс блоктары ретінде маңызды рөл ойнайды [28]. Бірнеше 1,3-дииндар синтетикалық органикалық химияда басқа функционалды топтарды алмастырғыш ретінде қолданылған. Сонымен қатар, 1,3- дииндар, көптеген табиғи қосылыстардан табылған көп

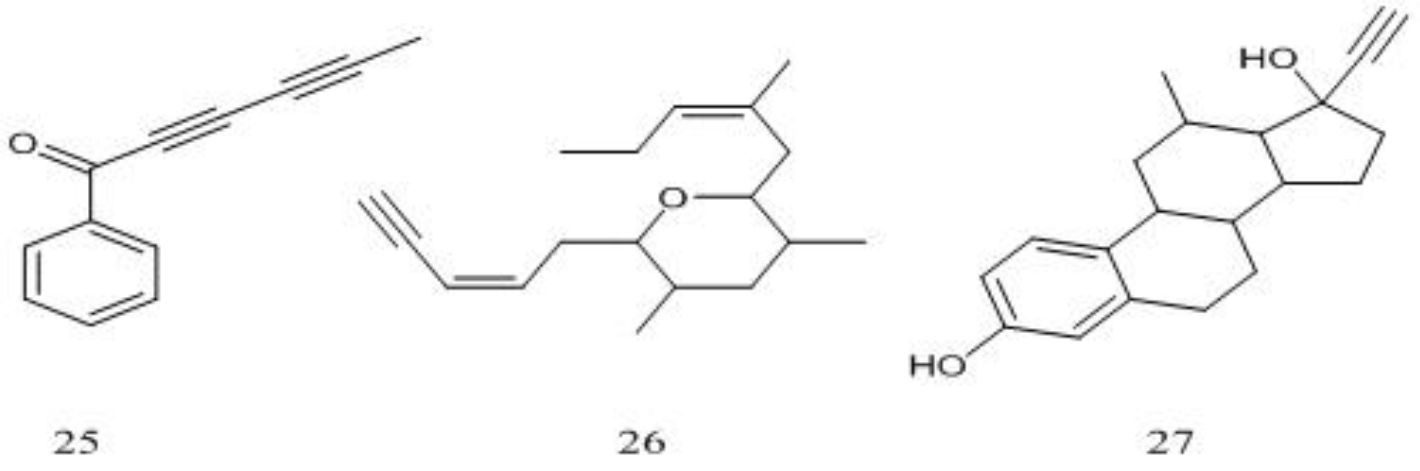
белсенділікке ие болғандығымен маңызды [30]. Сонымен қатар, көптеген алкиндер биологиялық қызығушылыққа ие, мысалы Каприллин 25 табиғаттан алынған
Жоғарыда келтірілген мәліметтер негізінде, ацетилен туындыларының түрленуі негізінен екі бағытта, үштік байланыстың бұзылуы немесе қозғалмалы сутектің қатысы арқылы жүретінін атап кеткен жөн.
Қорытынды. Қарасытырылған мысалдар негізінде ацетилен қосылыстарын түрлендіру саласында жан-жақты ізденістер жасалып жатқанын көрдік. Сондай жұмыстар нәтижесінде ацетилен туындыларын синтездеудің оңтайлы саңырауқұлақтарға қарсы препарат, Дактилин 26 теңізден алынған табиғи өнім, ал Этинил эстрадиол 27 синтетикалық эстроген болып табылады [31].
әдістемелері жасалған жәнежаңа биологиялық белсенді қосылыстар синтезделген. Алынған қосылыстар негізінен паразиттерге, микробтарға қарсы әсер көрсетіп, адамның жүйке жүйесіне қатысты ауруларды емдеуде қолданыс тапқан. Сонымен, осы шолудан ацетилен туындыларыныңсинтетик ғалымдардың ерекше назарына ие екенін қорытындылауға болады.
ӘДЕБИЕТТЕР ТІЗІМІ
- Садыков Т.С., Курманкулов Н.Б., Ержанов К.Б. Изучение регионаправленности взаимодействия N-метил-N- фенилпропаргиланилина с 1,2,5-триметил-4-кетопиперидином в суперосновной среде // Изв. НАН РК. Сер. хим. – 1995. – № 5. – С. 14-18.
- Бадмаева И.А., Суровцев Н.В., Малиновский В.К., Свешникова Л.Л. Исследование методами ИК и КР спектроскопии фотополимеризации пленок Ленгмюра-Блоджетт ацетиленовой кислоты // Журнал структурной химии. - 2010. - Т. 51. - № 2. - С. 259-265.
- Курманкулов Н.Б. Регионаправленность взаимодействия N-метил-N-пропаргиланилина с циклогексаноном и 1,2,5- триметилпиперидин-4-оном в сверхосновной среде // Труды ИХН МОН РК «Химия природных и синтетических биологически активных веществ (строение, превращения и свойства). – Алматы: 2001. – Т. 76. – С. 176-184.
- Котляревский И.Л., Шварцберг М.С., Фишер Л.Б. Реакции ацетиленовых соединений. – Новосибирск: Наука, 1967. – С.356.
- Бидусенко И.А. Реакции третичных пропаргиловых спиртов в суперосновных средах: циклодимеризация, ацетализация, винилирование: автореф. канд. хим. наук. – Иркутск: 2013. - 22 с.
- Бутин Б.М., Логунов А.П., Курманкулов Н.Б. Ирдан Нигметович Азербаев // Труды Межд. конф. «Состояние и перспективы развития органической химии в Республике Казахстан», посвященной 90-летию член-корр. АН КазССР И.Н.Азербаева. – Алматы-Шымкент: 2002. – С. 5-18.
- Ержанов К.Б., Визер С.А., Курманкулов Н.Б. Научный вклад лаборатории химии физиологически активных соединений в развитие химии ацетиленовых и гетероциклических соединений // Хим. журн. Казахстана. Â 2005. - № 4. - С.208-239.
- Басымбеков М.Б., Ержанов Қ.Б. Өсімдік өсуін реттегіштер – Алматы: Кайнар, 1995. – 176 с.
- Рубина К., Флейшер М., Абеле Э., Попелис Ю., Лукевиц Э. Прототропная перегруппировка N-, O- и S-пропаргилпроизводных гетаренов в условиях межфазного катализа: механизм и ограничения // Ж. Орг. Хим. – 2003. – Т. 39, № 7. – С. 1024-1028.
- Zindo F.T., Quinton R.B., Joubert J., Bergh J.J., Petzer J.P., Malan S.F. Polycyclic propargylamine and acetylene derivatives as multifunctional neuroprotective agents // European Journal of Medicinal Chemistry. – 2014. – vol. 80. - P. 122-134.
- SemwalAbha, Bhattacharya Arunasis, NayakSandip K. Ultrasound mediated selective monoalkylation of 4-tert-butylcalix[6]arene at the lower rim // Tetrahedron. – 2002. – Vol. 58, № 26. – P. 5288-5290.
- Altman R.A., Shafir A., Choi A., Lichtor Ph. A., Buchwald S.L. An Improved Cu-Based Catalyst System for the Reactions of Alcohols with Aryl Halides // J. Org. Chem. – 2008. – Vol. 73, N 1. – P. 284-285.
- Balasubramanian K.K., Venugopalan B. Studies in the Claisen rearrangement. Claisen rearrangement of bispropargyl ethers //Tetrahedron Lett. – 1973. – Vol. 29. – P. 2707-2710.
- Ariamala G., Balasubramanian K.H. A simple route for the synthesis of 4-chlorochromenes and chroman-4-ones // Tetrahedron Lett. – 1988. – Vol. 29, № 28. – Р. 3487-3488.
- Ahluwalia Vinod K., Prakash Chandra, Jolly Ravinder S. Synthesis of linear 3-phenylpyranocoumarins: Synthesis of robustin, robustic acid, and their methyl ethers //J. Chem. Soc. Perkin Trans.1. – 1981. – № 6. – P. 1697-1702.
- Садыков Т., Ержанов К.Б., Басымбеков М.Б., Пралиев С.Д. Гидратация о-, м-, п-ди(пропинилокси)бензолов и их гликолей // Изв. АН КазССР. Сер. хим. – 1988. – № 1. – С. 63-67.
- Басымбеков М.Б., Садыков Т.С., Адильбеков С.Т., Серикбаев К.С., Ержанов К. Синтез замещенных феноксипропинилпиперидолов и влияние заместителей на строение продуктов, полученных в условиях реакции гидратации // Изв. АН РК. Сер. хим. – 1992. – № 4. – С. 50-56.
- Ержанов К.Б. Функционально замещенные моно- и полиацетиленовые спирты: синтез, строение, превращения и ростстимулирующая активность: автореф. докт. хим. наук. – Алма-Ата: 1991. – 51 с.
- Otter B.A., Saluja S.S., Fox J.J. Pyrimidines. XII. A propargyl claisen rearrangement in the pyrimidine series. Synthesis of Furo- and Pyrano[3,2-d]pyrimidines // J. Org. Chem. - 1972. - Vol. 37, N 18. - P. 2858-2860.
- Kenny R.S., Mashelkar U.C., Rane D.M., Bezawada D.K. Intramolecular electrophilic hydroarylation via Claisen rearrangement: synthesis of cromenes, heterothiochromenes and heterodihydrothiochromenes // Tetrahedron. - 2006. - Vol. 62. - № 39. - P. 9280-9288.
- Dahlen A., Petersson A., Hilmersson G. Diastereoselective intramolecular SmI2-H2O-amine mediated couplings // Org. and Biomol. Chem. - 2003. - Vol. 1, № 14. - С. 2423-2426.
- Abad A., Agullo C., Cunat A.C., Llosa M.C. Stereoselective construction of the tetracyclic scalarane skeleton from carvone // Chem. Commun. - 1999. - № 5. - P. 427-428.
- Пат. 6538685 В2 США.Compositions containing and methods of using 1-aminoindan and derivatives thereof and process for preparing optically active 1-aminoindan derivatives. // Опубл. 04.03.03.
- Кияшев Д.К., Кулумбетова К.Ж., Ержанов А.И., Абиюров Б.Д. Каталитическое гидрирование ацетиленовых и диацетиленовых производных 2,6- дифенилтетрагидротиопиран-4-она // Изв. АН КазССР. Сер.хим. -Алма-Ата: 1979. - № 6. - С. 73-76.
- Курманкулов Н.Б. Гетеро(N-, O-, S-)атомные пропаргильные соединения в качестве химических средств защиты и регуляторов роста растений // Пищевая технология и сервис - 2008. - № 4. - С. 51-56.
- Anisimov A.V., Viktorova E.A. Thio-claisen rearrangement in the synthesis of sulfur-containing heterocyclic compounds // Chem. Heterocyclic Comp. - 1980. - Vol. 16, № 4. - Р. 321-333.
- Пат. 4218467 США. 8-Methoxy-3-phenyl-5-methyl-propargylamino-methyl-2H-1-benzopyran-2-one and pharmaceutical compositions containing it. // Опубл. 19.08.80.
- Визер С.А., Ержанов К.Б. Производные 4-ариламино-2-бутиновых кислот как вещества с потенциальной фармакологической активностью. Тезисы докл. научно-практ. конф. "Технология возделывания, переработка лекарственного сырья и производство фитопрепаратов для медицины и сельского хозяйства". - Алматы: НИЦ "Бастау". - 1997. - С. 115.
- Dzhalmakhanbetova R.I., Ivasenko S.A., Kulyyasov A.T., Khasenov B.B., Adekenov S.M., Kurmankulov N.B. Phosphorus derivatives of natural lactones. Synthesis of new grosshemin dialkylphosphonates // Chemistry of Natural Compounds. - 2004. - Vol. 40, N 4. - P. 381386.
- Ивасенко С.А., Джалмаханбетова Р.И., Кулыясов А.Т., Курманкулов Н.Б., Адекенов С.М. Строение промежуточного продукта в реакции присоединения диалкилфосфористых кислот к гроссгемину // ХПС. - 2004. - № 4. - С. 316-318.
- Шемякин М.М., Хохлов А.С. Химия антибиотиков. - М.: АН СССР, 1961. - 774 с.