Аннотация
Римантадин субстанциясының, сонымен қатар оның дәрілік түрлерінің физикалық және химиялық қасиеттері салыстырмалы түрде зерттеліп, олардың сандық мөлшерін анықтайтын бірыңғайланған фотоколориметриялық әдістемесі жасалды. Статистикалық өңдеу нәтижелері бірыңғайланған сандық анықтау әдістеменің қайталанғыштығын, сызықтық тәуелділігін, салыстырмалы дәлдігін көрсетті. Әдістеменің орташа салыстырмалы қателігі ±1,55-2,92 % аралықты көрсетуі жасалған әдістеменің сенімді-лігін дәлелдейді.
Кілт сөздер: римантадин, фотоколориметрия, бірыңғайлау, валидация.
Соңғы жылдары қарқынды дайындалып жатқан дәрілік заттардың ішінде вирусқа қарсы қолданылатын препараттар алдыңғы орындар қатарына жатады. Көптеген зерттеулер нәтижесі кең тараған инфекциялық аурулар - грипп, ВИЧ инфекциясы және көптеген өткір респираторлық вирустық инфекциялар (ОРВИ), гепатит, герпес инфекцияларын емдеуге қолданылатын жаңа дәрілік препараттарды іздеу және зерттеу керек екендігін көрсетті.
Жоғарыда аталған аурулардың алдын алу және емдеу үшін қолданылатын препараттардың бірі римантадин болып табылады. Римантадин - адамантан туындысы, вирусқа қарсы қолданылатын препарат, A типті грипп вирусының әртүрлі штаммдарын (A - H1N1, H2N2 және H3N2) , Herpes simplex I және II типті вирустарын, Flaviviridae тұқымдастарына жататын арбовирустарды емдеуде қолданады, сонымен қатар антитоксикалық және иммуномоделдеуші әсерлер көрсетеді [13].
Медицинада римантадиннің субстанциясымен қатар оның әртүрлі дәрілік түрлері (римантадин таблеткалары, 50 мг, римантадин капсулалары, 100 мг кеңінен қолданылады. Нормативті құжаттар бойынша римантадинді және оның дәрілік түрлерін талдауда сусыз ортадағы нейтрализация, дифференциалды спектрофотометрия, сұйықтық хроматография әдістері қолданылады [4-6].
Аталған әдістердің өзіне тән кемшіліктері бар. Мысалы сусыз ортада титрлеу әдісін жүргізу үшін арнайы мамандандырылған аналитик қажет, сонымен бірге бұл әдісте өте улы және ұшқыш заттар, мысалы мұзды сірке қышқылы, хлорлы сутек қышқылы қолданылады, жұмыс жасау арнайы жабдықтарды қажет етеді. Аталған кемшіліктерді ескере отырып, зерттеулер нәтижесінде қол жетімді, эффективті және экономикалық жағынан тиімді бірыңғайланған әдістемелер жасау өзекті мәселе болып табылады.

Дәрілік заттарды талдау әдістерін бірыңғайлау - дәрілік заттарды талдаудың жүйелі әдістерін жасау, аналитикалық бақылау әдістерін қарапайым ету, талдау уақытын және қолданылатын реагенттер санын төмендету, яғни еңбек өнімділігін арттырады және экономикалық тұрғыдан алғанда тиімді. Бірыңғайлау нәтижесінде дәрілік заттардың сапасы, дәрілік терапияның сенімділігі және эффективтілігі жоғарылайды.
Жұмыстың мақсаты. Римантадин субстанциясын және оның дәрілік түрлерін талдау үшін бірыңғайланған фотоколориметрия әдістемесін жасау.
Материалдар және әдістер. Жұмыстаримантадиннің дәрілік субстанциясы («Shanghai Xiandai Hasen (Shanggiu) Pharmaceutical Co.,Ltd.», Қытай); римантадиннің таблеткалары 50 мг, (Белоруссия Республикасы, Борисов зауыты, АНД РК 42-6639-14); қосымша заттар: лактоза моногидраты (ҚР МФ, т.1, 380б) , картоп крахмалы (ҚР МФ, т.1, 373б), тальк (ҚР МФ, т.1, 422б), стеарин қышқылы (ҚР МФ, т.2, 465 б).
Натрий нитропруссиді 1 % ерітіндісі, 0,1 М натрий гидроксиді ерітіндісін ҚР МФ сай жасалынды. Қолданылған реактивтер мен ерікіштер «т.ү.т» квалификациясына сай.
Римантадиннің натрий нитропруссидімен әрекеттескен өнімінің көрінетін аймақтағы спектрін зерттеу. 0,1 г (нақты өлшем) римантадин ұнтағын 50 мл өлшеуіш колбаға енгізіп, 20 мл тазартылған суда ерітіп, сумен белгісіне дейін жеткізеді (А ерітіндісі).
Дайындалған А ерітіндісінен 5 мл алып, сыйымдылығы 25 мл колбаға енгізіп, оған 2 мл 1% натрий нитропруссиді ерітіндісін, 2 мл ацетон ерітіндісін және 0,2 мл 10% натрий карбонаты ерітіндісін құйып, 40 минутқа қалдырады.
Ерітіндіні белгісіне дейін жеткізіп, оптикалық тығыздығын қалыңдығы 10 мм кюветада, 400700 нм толқын ұзындығы аймағында спектро-фотометрде өлшейді. Зерттеу нәтижесінде алынған өнім 537±2 нм аймағында жұтылу максимумын берді (Сурет 1).
Калибровты графикті құру. 0.0125; 0.025; 0.05; 0.075; 0.1; 0.15 г римантадин субстанциясын 100 мл өлшегіш колбаға енгізіп, 20 мл тазартылған суда ерітіп, сумен белгісіне дейін жеткізеді. (А ерітінді).
Дайындалған А ерітіндісінен 5 мл алып, сыйымдылығы 25 мл колбаға енгізіп, оған 2 мл 1% натрий нитропруссиді, 2 мл ацетон және 0,2 мл 10% натрий карбонаты ерітінділерін құйып, 40 минутқа қалдырады.
Ерітіндіні белгісіне дейін жеткізіп, оптикалық тығыздығын қалыңдығы 10 мм кюветада 537±2 нм толқын ұзындығында спектрофотометрде өлшейді.
Зерттелетін ерітіндімен қатар римантадиннің 0,01% жұмысшы стандарт үлгісі (ЖСҮ) ерітіндісінің оптикалық тығыздығын өлшейді. Салыстыру ерітіндісі ретінде тазартылған су қолданылады.
Римантадин таблеткаларының,50 мг талдау әдістемесі. 1 таблетканы (нақты өлшем) 10 мл өлшеуіш колбаға енгізіп, 20 мл тазартылған суда ерітіп, сумен белгісіне дейін жеткізеді (А ерітіндісі). Дайындалған ерітіндіні фильтрлеп, алдыңғы 10-15 мл алып тастайды.
Дайындалған А ерітіндісінен 5 мл алып, сыйымдылығы 25 мл колбаға енгізіп, оған 2 мл 1% натрий нитропруссиді ерітіндісін, 2 мл ацетон ерітіндісін және 0,2 мл 10% натрий карбонаты ерітіндісін құйып, 40 минутқа қалдырады.
Ерітіндіні белгісіне дейін жеткізіп, оптикалық тығыздығын қалыңдығы 10 мм кюветада 537±2 нм толқын ұзындығында спектрофотометрде өлшейді.
Дайындалған ерітіндіні және ЖСҮ ерітіндісін жоғарыдағыдай субстанцияның зерттеу әдістемесі бойынша анықтайды.
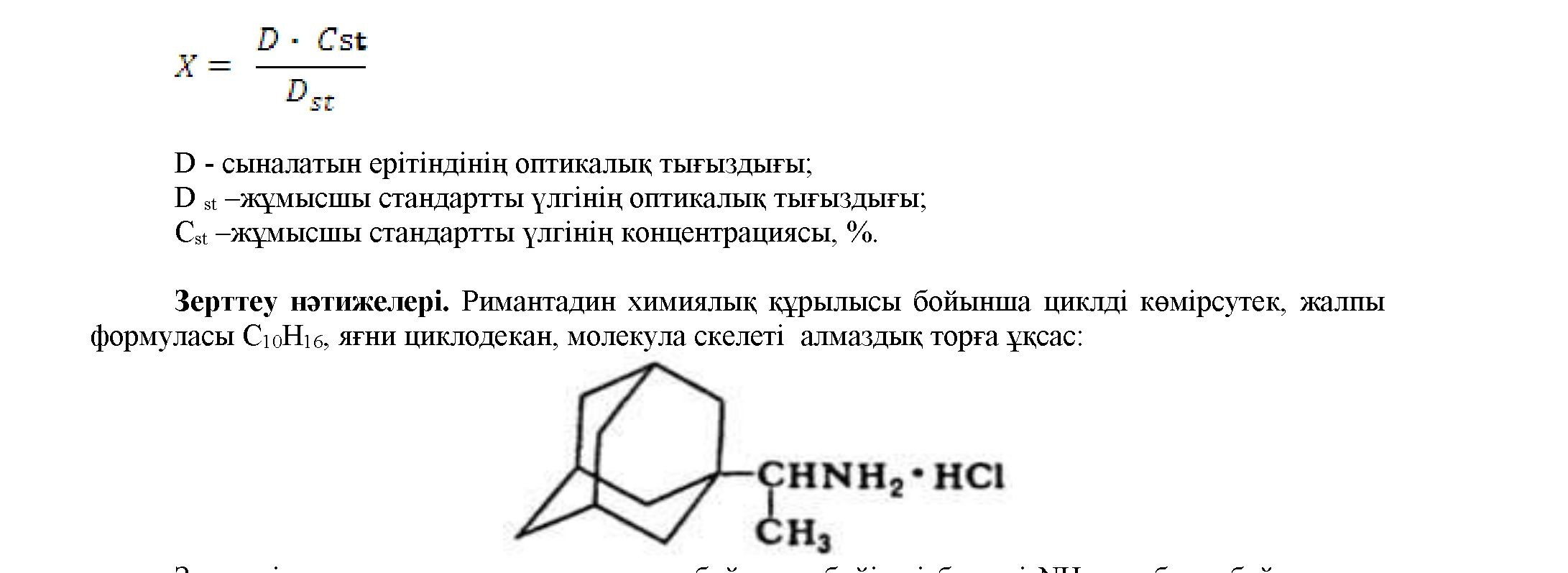
Римантадиннің таблеткадағы мөлшері (мг) келесі формуламен есептеледі:
зерттеліп отырған препарат құрылысы бойынша бүйір тізбектегі NH2 — тобына байланысты аминоқышқылдарына тән нингидринмен, натрий нитропруссидімен түрлі-түсті реакцияларды түзеді.
Римантадиннің натрий нитропруссидімен түзілген түсті өнімі бойынша оның сандық анықтауын көрінетін аймақтағы спектрофотометрия әдісімен анықтау - римантадин субстанциясына және оның дәрілік түрлеріне бірыңғайланған фотоколориметрия әдістемесін жасаудың негізі болып табылды.
Реакцияны препараттың идентификациясын және сандық анықтауын
фотоэлектроколориметрия әдістерімен анықтауда қолдануға болады. Жұтылу максимумының оптикалық тығыздығы зерттелген препараттың сандық мөлшеріне тәуелді. Осы реакция римантадиннің барлық дәрілік түрлеріне бірыңғайланған әдістеме жасау мақсатында қолданылды.
Аналитикалық әдістемені бағалаудың негізгі критерийі - валидациялау болып табылады.
Әдістеменің валидациясы өзара байланысты жүйелік сипаттамалар - спецификалықты, сызықтықты, дұрыстықты және қайталанғыштықты анықтауды талап етеді. Әдістемені валидациялау Қазақстан Республикасы Мемлекеттік фармакопеясы талаптарына сәйкес жүргізілді [7].
Әдістің сызықтық тәуелділігі сыналатын үлгідегі талданатын заттар мөлшеріне тура пропорциональды оптикалық тығыздықты аналитикалық сигнал түрінде алу қабілетімен сипатталады. Сызықтығы модельді қоспада римантадиннің рұқсат етілген мөлшері 0.0025-0.0300 % аралығында зерттелді.
Калибровты график бойынша римантадин субстанциясының оптикалық тығыздығы оның концентрациясына тәуелді екені жарықты жұту Бугер-Ламберт-Бэр заңына сай келеді, сызықтық тәуелділік у=вх+а теңдеуімен сипатталады. Сызықтық регрессиялық графиктің корреляция коэффициенті r 0,9988 құрады (Сурет 2).
76
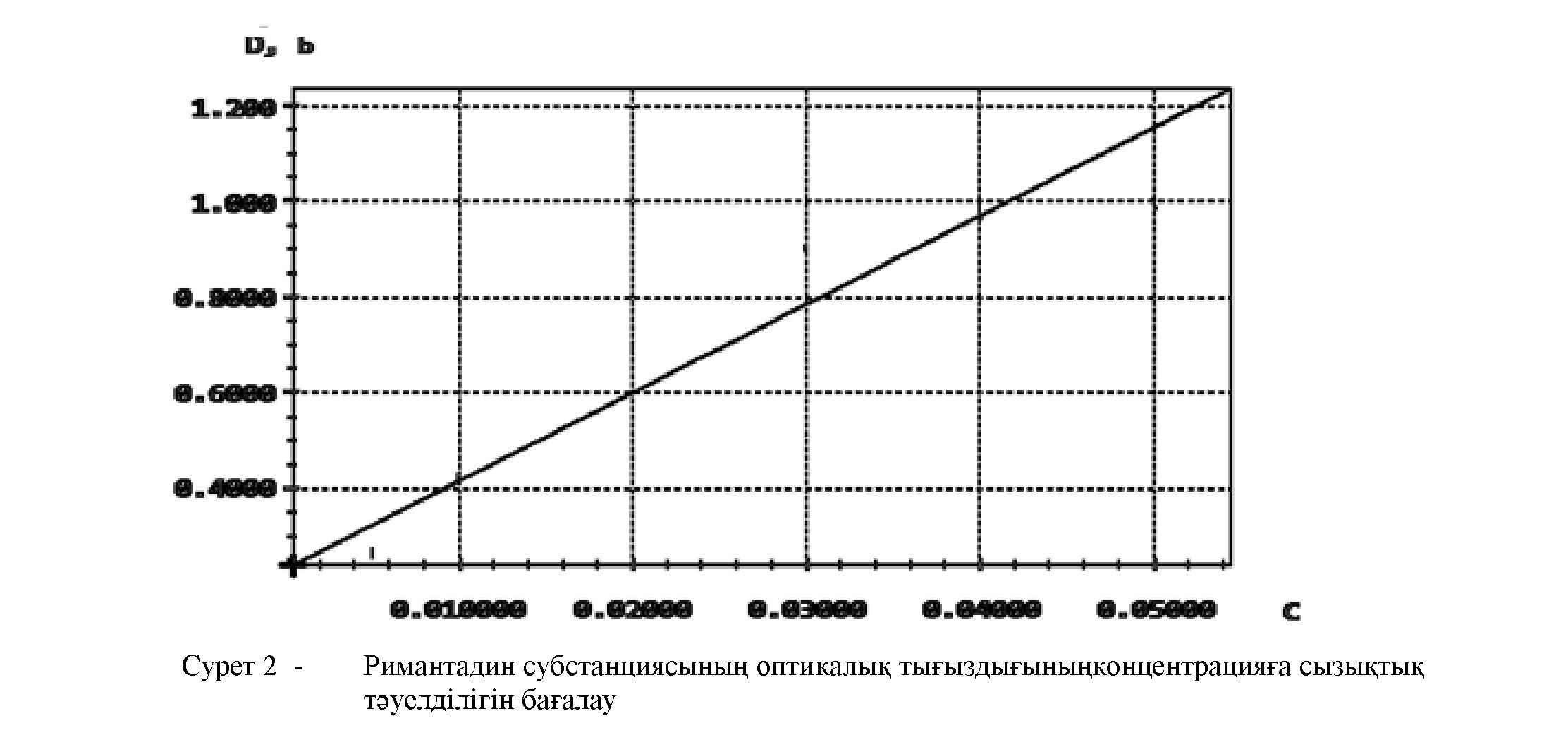

Алынған нәтижелер негізінде римантадин субстанциясының оптикалық тығыздығының концентрацияға сызықтық тәуелділігі жіберілетін мөлшер шамасының аралығы 0,025-0,3 мг/мл құрады. Осы шама әдістеменің аналитикалық аймағы болып табылады (Кесте 1).
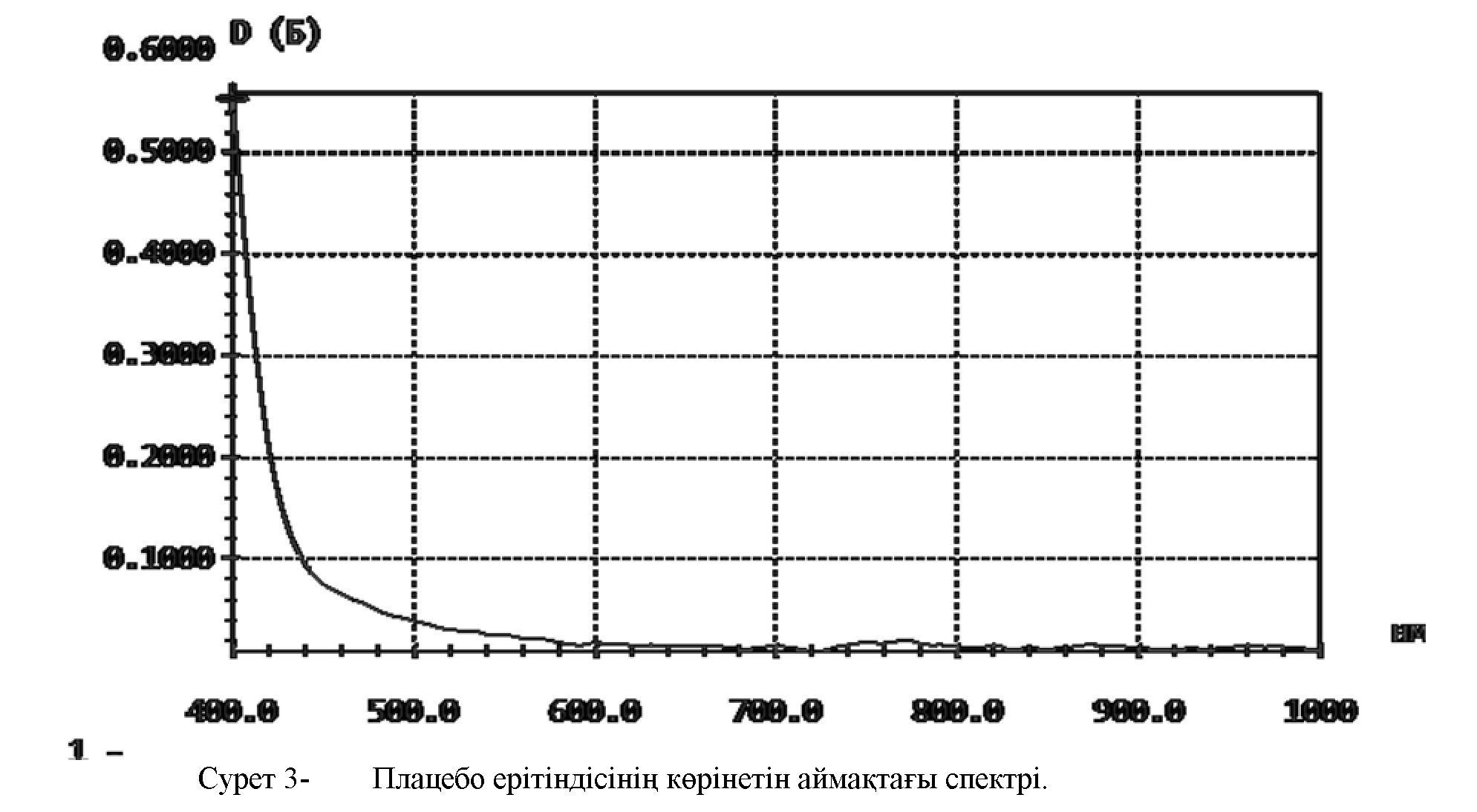
Әдістеменің спецификалығы римантадиннің 537±2 нм толқын ұзындығында жарықты жұту максимумын беруімен сипатталады. Бұл үшін 5 сериялы плацебо ерітінділері дайындалып, олардың жарықты жұту қабілеті зерттелді. Зерттеулер нәтижесінде дайындалған плацебо ерітінділерінде электромагнитті толқынды жұтыуы байқалмады, оптикалық тығыздықтың мәні 0,05-тен аспады, яғни қосымша заттар анықтауда кедергі жасамайды (Сурет 3).
77
Әдістеменің дұрыстығы (дәлдігі) модельді қоспалардағы римантадиннің белгілі концентрацияларына талдау жүргізу арқылы орындалды. Бұл параметрлерді анықтау барысында концентрациясы белгілі стандартты үлгілердегі римантадин мөлшері мен табылған мөлшер арасындағы байланысты көрсетеді. Жасалған бірыңғайланған әдістеменің дұрыстығы үш реттік анықтауға стандартты үлгілердің 5 аналитикалық концентрациясын қолдана отырып, 80-120% аралығында модельді қоспаларға талдау жүргізу арқылы дәлелденді. 2 кестеде көрсетілген зерттеу нәтижелері әдістеменің дәлдігін сипаттайды. Әдістеменің дұрыстығын әдістің жүйелі қателігін және талданатын үлгінің дәл өлшенген санын регенерация пайызы түрінде көрсетті.
Аналитикалық әдістеменің қайталанғыштығы римантадинді бірнеше рет жеке анықтауда нәтижелердің сәйкес келу дәрежесімен сипатталады. Дәрілік субстанция құрамындағы анықталған римантадин үшін орташа салыстырмалы қателіктің ± 1,55 % аралықты көрсетуі және, «Римантадин таблеткалары 50 мг» үшін орташа салыстырмалы қателіктің ± 2,92 % аралықты көрсетуі жасалған әдістеменің сенімділігін дәлелдейді (3, 4 кестелер).
 78
78
Кесте 3- Римантадин субстанциясына арналған біріңғайланған әдістемесінің қайталанғыштығын бағалау
|
Римантадиннің табылған мөлшері, % |
Метрологиялық сипаттамалары (ҚР МФ т. 1, 100б.) |
||||||
|
n |
Хор |
S |
Ахор |
R, f |
±АХор |
е ор ,% |
|
|
98,23 |
9 |
99,86 |
1,672 |
0,55 |
2,45 |
1,549 |
1,55 |
|
99,65 |
|||||||
|
100,28 |
|||||||
|
99,34 |
|||||||
|
101,56 |
|||||||
|
101,99 |
|||||||
|
98,32 |
|||||||
|
101,89 |
|||||||
|
97,53 |
|||||||
Кесте 4- Зерттелген римантадин таблеткаларына 50 мг арналған біріңғайланған әдістемесінің қайталанғыштығын бағалау
|
Римантадиннің табылған мөлшері, г |
Метрологиялық сипаттамалары (ҚР МФ т.1, 100б.) |
||||||
|
n |
Хор |
S |
Ахор |
R, f |
Хор±Ахор |
£ор,% |
|
|
0,05201 |
9 |
0,04971 |
0,00156 |
0,00052 |
2,45 |
0.00145 |
2,92 |
|
0,04729 |
|||||||
|
0,04992 |
|||||||
|
0,04743 |
|||||||
|
0,05199 |
|||||||
|
0,04749 |
|||||||
|
0,05198 |
|||||||
|
0,04750 |
|||||||
|
0,05179 |
|||||||
Қорытынды: Римантадиннің субстанциясына және «Римантадин таблеткалары, 50 мг» дәрілік түрін талдауға валидирленген фотоэлектроколориметрия әдістемесі жасалынды. Жасалынған әдістемені дәрілік препараттың сапасын бақылауда альтернативті әдіс ретінде ұсынуға болады.
Қолданылған әдебиеттер
- .Шульдякова О.Г. Инфекционные болезни): диссертация канд м. наук.: г.Саратов.- СГМУ.-2007.-С. 147.
- . Усубаев М.У., Якубджанова.М.Ш., Тошкулова Ф. Разработка технологии таблеток на основе римантадина и оценка качественных показателей //Фармацевтический журнал.-2004.-№3.-С. 14-15.
- . Якубджанова М.Ш., Усуббаев М.У., Нурмухамедова М.Х.. Разработка и технология антивирусного препарата на основе римантадина. //Междун. научн. конф. «Химия природных и синтетических биологически активных соединений».- Алматы, 2004.-С.397-400.
- .Якубджанова М.Ш., Назаров Э.А., Усубаев М.У. Валидация методов количественной оценки многокомпонентного препарата «Римантадин-ПС» // Фармацевтический журнал.-2006.-№1-2.-С. 4651.
- .Курбатова С.В.Газовая хроматография производных адамантана: Диссертация доктора м. наук.: г.Самара.- 2000.-С. 295.
- .ФС РК 42-630-04 Римантадина гидрохлорид.
- .Қазақстан Республикасының Мемлекеттік фармакопеясы.-Алматы: «Жібек жолы» баспа үйі.- 2008.-1 Т.-592б.
- .Қазақстан Республикасының Мемлекеттік фармакопеясы.-Алматы: «Жібек жолы» баспа үйі.-2009.-2 Т.-804б.
- .Қазақстан Республикасының Мемлекеттік фармакопеясы.-Алматы: «Жібек жолы» баспа үйі.-2014.-3 Т.-709б.
- . АНД РК 42-6639-14.- Римантадин таблеткасы 50 мг.- «Борисовский завод медицинских препаратов» (ОАО «БЗМП»).- Республика Беларусь.-2014.
- . British Pharmacopoeia (BP 2016). - London The Stationery Office.-2016.
- . European Pharmacopoeia 8.4.- EDQM.-2015.