Аннотация
Азитромициннің оригиналды препараты Сумамед® 250 капсуласы мен оның дженерика- лық препараттары Азитро® 250 және Азитромицин 250 капсулаларының фармацевтикалық эквиваленттілігі Қазақстан Республикасының Мемлекеттік Фармакопеясының талаптары бойынша бағаланды. Фармацевтикалық эквиваленттілікті бағалау үшін азитромицин капсуласының идентификациясы, «еру» тесті, тектес қоспалары, микробиологиялық тазалығы, сандық мөлшері сынды параметрлер бойынша талдау жүргізілді. Зерттеу нәтижесінде алынған оригиналды және дженерикалық препараттардың сандық мөлшерінің мәндері Стьюдент критерийімен статистикалық өңделіп, сенімділігі дәлелденді. Зерттеу нәтижесінде салыстырмалы препарат Сумамед® 250мг капсуласы мен оның сыналатын препараттары Азитро® 250мг және Азитромицин 250мг капсулаларының Қазақстан Республикасының Мемлекеттік Фармакопеясы талаптарына сай фармацевтикалық эквивалентті екені дәлелденді.
Кілтті сөздер: Азитромицин, өзараалмасушылық, фармацевтикалық эквиваленттілік, дженерикалық дәрілік құралдар, оригиналды дәрілік құралдар
Кіріспе. Дженерикалық дәрілік құралдармен қаныққан нарық заманында өзараалмасушы- лық, яғни оригиналды препаратты оның көшірмесіне ауыстыру мәселесі қаржыларды тиімді қолдану мәселесі болғандықтан, мемлекеттің бюджетінен бөлінетін қаржыларды тиімді сатып алуды ұйымдастыруда үлкен мәнге ие. Өйткені республикалық және аймақтық қаржылардың тиімді жұмсалуы мәселелері билікті жаңа, тиімдірек және де арзанырақ препараттарға назарын аудартып отыр. Бұған Қазақстан Республикасының фармацевтикалық нарығының құрылымының 86,4% дженерикалық препараттарға тиесілі екені дәлел бола алады [3]. Сонда да ДП “эквиваленттілігі” түсінігінің орнына ұсынылған “өзаралмасушылық” терминінің бір мәнді еместігі біріздендірілген сатып алу кезінде әжептеуір қиындық тудырады.
Өйткені дженерикалық препараттар да инновациялық (оригиналды) препараттар сияқты бірыңғай техникалық құжаттарда берілген жалпы талаптарға тиімділігі, қауіпсіздігі, сапасы бойынша жауап беруі керек. Егер де алғашқы екі категория медико-биологиялық сұрақтарға жатса, ал сапасы нағыз фармацевтикалық мәселеге жатады. Себебі дәрілік заттың
фармацевтикалық сипаттамасы оның әрі қарай айналым кезіндегі тағдырын анықтайды, өйткені клиникаға дейінгі және клиникалық зерттеу бір-ақ рет жүргізіледі және дәрілік затты тіркеуден кейін мүлдем қайталанбайтынын атап өту керек [6,7].
Эквиваленттілікті бағалауда антибиотиктер ерекше назарды аудартып отыр. Солардың ішінде соңғы буындағы антибиотиктердің бірі азитромицин болып табылады. Азитромицин - кең спектрлі, бактериостатикалық әсерлі, жартылай синтетикалық антибиотик [5]. Қазақстан Респуб- ликасының фармацевтикалық нарығында оның таблетка, капсула, суспензия инъекцияға арналған ұнтақ түріндегі формалары кездеседі [4].
Зерттеу мақсаты. Сумамед капсулалары мен оның дженерикалық препараттарының фармацевтикалық эквиваленттілігін бағалау.
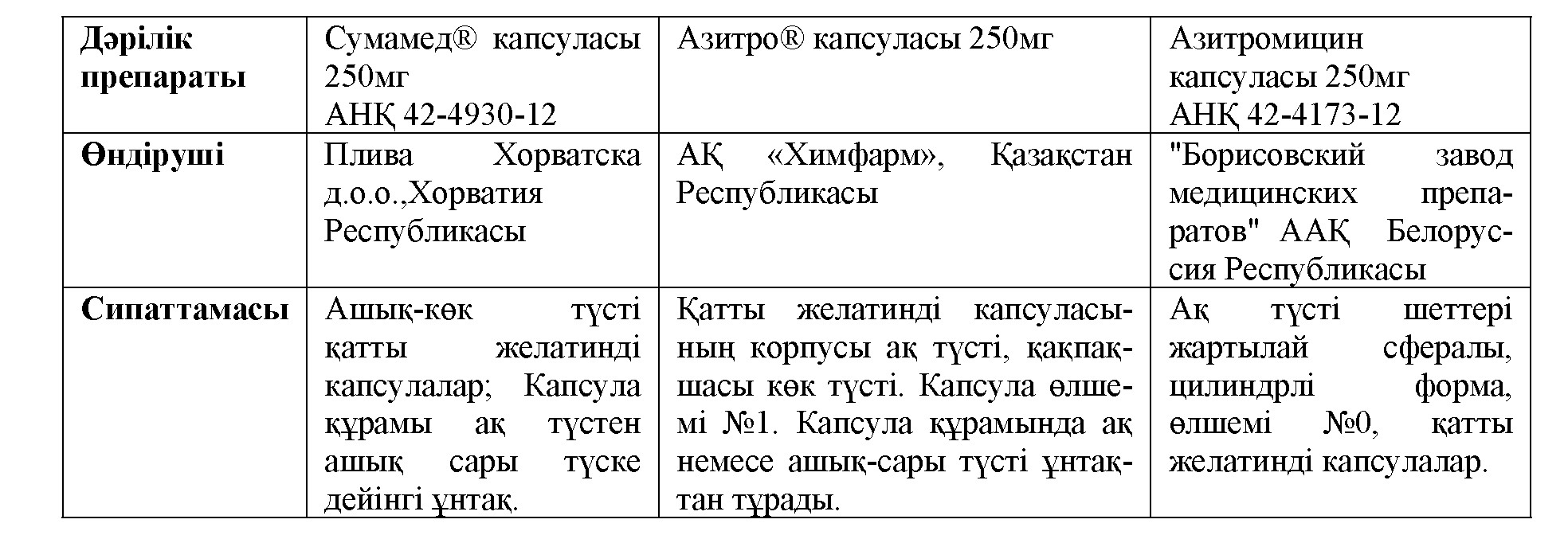
Кесте 1 - Дәрілік препараттардың сипаттамасы
Материалдары мен әдістері. Зерттеу объектілері ретінде Сумамед® 250мг, Азитро® 250мг, Азитромицин 250мг капсулалары алынды. Фармацевтикалық эквиваленттілікті бағалау үшін Қазақстан Республикасының Мемлекеттік Фармакопеясының 2 томындағы азитромицин капсуласына арналған фармакопеялық мақалаға сай жүргізілді. Онда препараттың идентифи- кациясы, «еру» тесті, тектес қоспалары, микробиологиялық тазалығы, сандық мөлшері сынды параметрлері бойынша талданды. Зерттеу кезінде физикалық-химиялық, микробиологиялық және биофармацевтикалық әдістер қоданылды. Физикалық-химиялық әдіс жоғары эффективті сұйық- тық хроматография әдісін идентификация, тектес қоспалары және сандық мөлшеріне сынау жүргізгенде қолданылды. Микробиологиялық тазалығына сынауға микробиологиялық әдіс, ал «еру» тестін жүргізу үшін биофармацевтикалық әдіс қолданылды [1,2]. Зерттеу объектілерінің толық сипаттамасы 1 кестеде берілген.
Нәтижелері мен талқылаулар. Құрамында дәрілік заттың дозасы бірдей, фармакопеяның және басқа да НТҚ талаптарына, физикалық-химиялық стандарттарға толық жауап беретін бірдей дәрілік түрде шығарылатын, бірақ әр түрлі тәсілдермен немесе әр түрлі кәсіпорындарда алынған дәрі ғана фармацевтикалық эквивалентті болып табылады.
Дәрілік препараттардың фармацевтикалық эквиваленттілігіне жүргізілген сараптама арқы- лы дәрілік препараттың үш басты сапалық көрсеткіштері дәрілік заттың өзі екендігі, тазалығы, сандық мөлшері Қазақстан Республикасының мемлекеттік фармакопеясында азитромицин капсуласына арналған мақала талаптарына сай анықталды.
Жүргізілген талдау мен оның нәтижелері 2 кестеде берілген.
Сонымен, дәрілік препараттың өзі екендігін анықтау арқылы дәрілік форма құрамындағы белсенді заттың өзі екенін дәлелденеді. Берілген дәрілік препараттарды жоғары эффективті сұйықтық хроматография әдісімен идентификациялағанда, азитромицин СҮЕ аудан шыңының ұсталу уақыты 1,63 болса, Сумамед капсуласының аудан шыңының ұсталу уақыты 1,63, Азитро капсуласында 1,61 және Азитромицин капсуласында 1,60 тең болғандықтан, олардың ұқсастығы дәлелденді.
«Еру» тесті сынауын ҚР МФ І, т. 2, 2.9.3 талаптарына сай қалақшалы құралмен жүргізілді. Еру ортасы - рН 6,8 фосфатты буфер, еру ортасының көлемі - 900мл, араластырғыштың айналу жылдамдығы - 100 айн./мин, еру ортасының температурасы - (37,0±0,5)0С, еру уақыты - 45 минут. Нәтижесінде босап шыққан дәрілік зат мөлшерін ультракүлгін және көрінетін аймақтағы
177абсорбциялық спектрофотометрия әдісімен анықтағанда, 45 минутта дәрілік препараттың 75% ыдырауы қажет.
Берілген дәрілік заттардың тазалығына сынау жүргізгенде, оның микробиологиялық тазалығы мен тектес қоспалардың мөлшерін анықтау сынды көрсеткіштер талданды.
Тектес қоспаларға жүргізілген сынауларда азитромицин В қоспасының мөлшері 2.0% аспады және де одан басқа қоспа түрлері анықталмағандықтан, Фармакопея талаптарына сәйкес болды.
Кесте 2 - Азитромициннің дәрілік препараттарының сапалық көрсеткіштері
Дәрілік препараттардың сандық мөлшерін анықтау арқылы әсер етуші заттың бір реттік дозасының дәлдігі анықталды. Алынған нәтижелер фармакопеялық талапта берілген нормаларға сәйкестігі дәлелденді [1,2].
2-кестеде берілген нәтижелерден оригиналды Сумамед және дженерикалық Азитро мен Азитромицин капсулаларының Қазақстан Республикасының Мемлекеттік Фармакопеясында берілген талаптарға сәйкестігі дәлелденді.
Оригиналды Сумамед® 250 капсуласы мен оның дженерикалық аналогтары Азитро® 250 және Азитромицин 250 капсулаларының сандық мөлшерін анықтауда алынған нәтижелер Стьюдент t-критерийін пайдалану арқылы статистикалық талданып, олардың сенімділігі дәлелденді. Алынған нәтижелер 3-5 кестеде берілген.
 178
178
Кесте 4 - Азитро® капсуласының сандық мөлшерін анықтау нәтижелері

3-5 кестелерде берілген нәтижелер қалыпты үлестіру кезінде Стьюдент t-критерийін қолдану арқылы алынды рП0,05 мәнділік дәрежесінде олардың нәтижелерінің сенімділігі дәлелденді.
Қорытынды.
- Зерттеу нәтижесінде азитромициннің оригиналды препараты Сумамед® 250мг мен оның дженрикалық препараттары Азитро® 250мг және Азитромицин 250мг капсулалары Қазақстан Республикасының Мемлекеттік Фармакопеясы талаптары бойынша идентификациясы, еру тесті, тектес қоспалары, микробиологиялық тазалығы, сандық мөлшері сынды параметрлері талданды. Салыстырмалы және сыналатын препарат та фармакопеялық мақалада берілген талаптарға сәйкес болды.
- Салыстырмалы препарат Сумамед® 250мг пен оның сыналатын препараттары Азитро® 250мг және Азитромицин 250мг капсулаларының сандық мөлшерін анықтағандағы нәтижелері Стьюдент t-критерийі бойынша сенімділігі дәлелденді.
- Зерттеу нәтижесінде салыстырмалы препарат Сумамед® 250мг капсуласы пен оның сыналатын препараттары Азитро® 250мг және Азитромицин 250мг капсулаларының Қазақстан Республикасының Мемлекеттік Фармакопеясы талаптарына сай фармацевтикалық эквивалентті екені дәлелденді.
Әдебиеттер
- Қазақстан Республикасының Мемлекеттік Фармакопеясы Т.1. - Алматы: «Жібек жолы» баспа үйі, 2008. - 592б.
- Қазақстан Республикасының Мемлекеттік Фармакопеясы Т.2. - Алматы: «Жібек жолы» баспа үйі, 2009. - 792б.
- Розиева К.Т. Обзор казахстанского рынка референтных препаратов антимикробного действия при лечении заболеваний органов дыхания /К.Т. Розиева, Г.Н. Имирова, Е.Н. Евтушенко, А.Р. // Вестник Казахского Национального медицинского университета.- 2015.-№1.-С.482-486.
- ГосударственныйреестрРКДL10.2016г-Режимдоступа:http://www.dari.kz/category/gos reestr excel
- А.В.Веселов. Азитромицин: современные аспекты клинического применения [Электронный ресурс]/А.В.Веселов,Р.В.Козлов//Клиническая микробиология и антимикробная химиотерапия.-2006.-Том8.-№1-С.18-32.- Режим доступа: http://www.antibiotic.ru/cmac/pdf/ 8_1_018.pdf
- Хосева Е.Н. Экономические преимуществаи слабые стороны генериков системе лекарственного обеспечения населения в России и за рубежом [Электронный ресурс] / Хосева Е.Н., Морозова Т.Е. // Качественная клиническая практика №2, 2013 г., с63-68.
- Оригинальные и воспроизведенные лекарственные средства - реалии современного фармацевтического рынка, - Режим доступа: http://www.remedium.ru/ state/ detail. php?ID= 46319& SHOWALL 1=0
- Государственная фармакопея СССР ХІ издания. -1989. - Том 1. -С,199-251.